题目内容
2.下列指定微粒的个数比为2:1的是( )| A. | Be2+中的质子和电子 | |
| B. | NaHCO3晶体中的阳离子和阴离子 | |
| C. | ${\;}_{1}^{2}$H原子中的中子和质子 | |
| D. | BaO2(过氧化钡)固体中的阴离子和阳离子 |
分析 A.Be2+离子中的质子和电子分别为4、2;
B.NaHCO3晶体中的阳离子和阴离子分别为Na+和HCO3-;
C.${\;}_{1}^{2}$H原子中的中子和质子分别为1、1;
D.BaO2固体中的阴离子和阳离子分别为Ba2+和O22-.
解答 解:A.Be2+离子中的质子和电子分别为4、2,二者个数比为2:1,故A正确;
B.NaHCO3晶体中的阳离子和阴离子分别为Na+和HCO3-,二者数目之比为1:1,故B错误;
C.${\;}_{1}^{2}$H原子中的中子和质子分别为1、1,二者数目之比为1:1,故C错误;
D.BaO2固体中的阴离子和阳离子分别为O22-、Ba2+,二者数目之比为1:1,故D错误,
故选A.
点评 本题综合考查物质构成、原子构成,注意对基础知识的理解掌握,D选项中注意根据过氧化钠进行迁移应用,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列有关实验操作的说法正确的是( )
| A. | 在水中加入KNO3固体,H2O?H++OH-的电离平衡向右移动 | |
| B. | 锅炉水垢中的CaSO4可用Na2CO3溶液浸泡后再用酸清洗 | |
| C. | 把锌粒放入盛有盐酸的试管中,加入几滴CuCl2溶液,气泡放出速率变慢 | |
| D. | 用铁片作阳极,锌片作阴极,电解ZnCl2溶液,铁片表面出现一层锌 |
13.下列做法,不能使CaCO3+2HCl═CaCl2+CO2↑+H2O的反应速率增大的是( )
| A. | 增大盐酸的浓度 | B. | 碾碎碳酸钙 | ||
| C. | 适当加热 | D. | 把盐酸换成同浓度硫酸 |
17.下列各组物质中互为同位素的是( )
| A. | ${\;}_{20}^{40}$Ca和${\;}_{18}^{40}$Ar | B. | ${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl | ||
| C. | H2O和H2O2 | D. | O3和O2 |
7.用NA表示阿伏德罗常数,下列叙述正确的( )
| A. | 标准状况下,22.4LH2O含有的分子数为1 NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 N | |
| C. | 通常状况下,1 NA个CO2分子占有的体积为22.4L | |
| D. | 标准状况下,22.4L CO2和SO2混合气中氧原子数为0.2NA |
2.下列电离方程式错误的是( )
| A. | NaHCO3=Na++H++CO32- | B. | NaOH=Na++OH- | ||
| C. | H2SO4=2H++SO42- | D. | KCl=K++Cl- |
20.原子序数为83的元素位于:①第5周期;②第6周期;③ⅣA族;④ⅤA族;⑤ⅡB族.其中正确的组合是( )
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①⑤ |
 有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.当加入0.4mol淡黄色粉末时,产生气体0.3mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如图所示.
有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.当加入0.4mol淡黄色粉末时,产生气体0.3mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如图所示.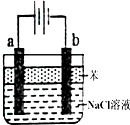 (1)用惰性电极电解饱和食盐水的反应方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(1)用惰性电极电解饱和食盐水的反应方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.