题目内容
12.下列有关实验操作的说法正确的是( )| A. | 在水中加入KNO3固体,H2O?H++OH-的电离平衡向右移动 | |
| B. | 锅炉水垢中的CaSO4可用Na2CO3溶液浸泡后再用酸清洗 | |
| C. | 把锌粒放入盛有盐酸的试管中,加入几滴CuCl2溶液,气泡放出速率变慢 | |
| D. | 用铁片作阳极,锌片作阴极,电解ZnCl2溶液,铁片表面出现一层锌 |
分析 A.硝酸钾电离出的钾离子和硝酸根离子都不影响水的电离;
B.碳酸钙比硫酸钙更难溶,可以加入碳酸钠将硫酸钙转化成碳酸钙沉淀;
C.锌与铜离子反应生成铜单质,生成的铜与锌形成原电池,大大加快了反应速率;
D.阳极铁溶解,溶液中氢离子得电子生成氢气,则电解过程中不会生成锌单质.
解答 解:A.在水中加入KNO3固体,钾离子和硝酸根离子都不水解,则H2O?H++OH-的电离平衡不移动,故A错误;
B.硫酸钙不与酸反应,而碳酸钙能够与酸反应,且碳酸钙比硫酸钙更难溶,故锅炉水垢中的CaSO4可先用Na2CO3溶液浸泡,然后再用酸清洗,从而达到除去水垢的目的,故B正确;
C.把锌粒放入盛有盐酸的试管中,加入几滴CuCl2溶液,铜离子被置换生成铜,则锌与置换出的Cu形成原电池,则产生气泡的速率加快,故C错误;
D.铁片作阳极,锌片作阴极,电解ZnCl2溶液,阳极铁片失去电子,则铁片质量减小,阴极上水电离的氢离子得到电子生成氢气,所以铁片上不会生成锌,故D错误;
故选B.
点评 本题考查难溶物溶解平衡及其影响、原电池工作原理、水的电离等知识,题目难度中等,试题涉及知识点较多,充分考查学生的分析、理解能力及灵活应用基础知识的能力,注意明确原电池、电解池工作原理及其应用,熟练掌握水的电离、弱电解质的电离平衡及其影响.

练习册系列答案
相关题目
2.在2A(g)+B(g)=3C(g)+4D(g)反应中,表示该反应速率最快的是( )
| A. | υ(A)=0.5 mol•(L•s)-1 | B. | υ(B)=0.3 mol•(L•s)-1 | ||
| C. | υ(C)=0.8 mol•(L•s)-1 | D. | υ(D)=1 mol•(L•s)-1 |
3.气体甲能使湿润的红色石蕊试纸变蓝,气体乙可在空气中产生白雾,当甲与乙相遇时可能生成( )
| A. | NH4C1 | B. | NH4HCO3 | C. | (NH4)2CO3 | D. | (NH4)2SO4 |
20.下列说法中不正确的是( )
| A. | 化石燃料在燃烧过程中会产生污染环境的CO、SO2等有害气体 | |
| B. | 直接燃烧煤不如将煤进行深加工后再燃烧的效果好 | |
| C. | 太阳能、氢能、风能、核能、天然气等都属于新能源 | |
| D. | 水煤气是一种二次能源,比煤直接燃烧污染小 |
7.下列有机物中,只含有一种官能团的是( )
| A. | 氯乙烯 | B. | 苯 | C. | 甲苯 | D. | 乙炔 |
17.下列关于有机物的叙述不正确的是( )
| A. | 甲烷、甲苯、乙醇、乙酸都可以发生取代反应 | |
| B. | 能发生银镜反应的有机物都是醛 | |
| C. | 乙酸乙酯在无机酸或碱存在时都能发生水解反应 | |
| D. | 可用浓溴水来区分乙醇和苯酚 |
2.下列指定微粒的个数比为2:1的是( )
| A. | Be2+中的质子和电子 | |
| B. | NaHCO3晶体中的阳离子和阴离子 | |
| C. | ${\;}_{1}^{2}$H原子中的中子和质子 | |
| D. | BaO2(过氧化钡)固体中的阴离子和阳离子 |
 如图是实验室进行“喷泉”实验的一种装置,使用下列物质一定不会出现“喷泉”现象的是( )
如图是实验室进行“喷泉”实验的一种装置,使用下列物质一定不会出现“喷泉”现象的是( )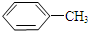 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$
 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$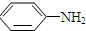

 ,G
,G .
. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O.
+H2O. 与碳酸氢钠溶液反应:
与碳酸氢钠溶液反应: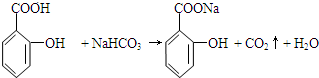 .
.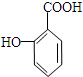 有多种同分异构体,其中属于芳香族化合物的同分异构体不可能为下列中的ad.
有多种同分异构体,其中属于芳香族化合物的同分异构体不可能为下列中的ad.