题目内容
【题目】氯化亚铜(CuC1)是白色粉末,微溶于水,酸性条件下不稳定,易生成金属Cu和Cu2+。某小组拟热分解CuCl2·2H2O制备CuC1,并进行相关探究。下列说法正确的是
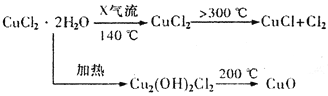
A. 制备CuC1时产生的Cl2可以回收循环利用,也可以通入饱和NaC1溶液中除去
B. Cu2(OH)2Cl2在200℃时反应的化学方程式为:Cu2(OH)2Cl2 ![]() 2CuO+2HCl↑
2CuO+2HCl↑
C. X气体可以是N2,目的是做保护气,抑制CuCl2·2H2O加热过程可能的水解
D. CuC1与稀硫酸反应离子方程式:2CuCl+4H++SO42-=2Cu2++2Cl-+SO2↑+2H2O
【答案】B
【解析】
A.Cl2在饱和NaC1溶液中的溶解度小,不能被吸收;
B.Cu2(OH)2Cl2加热至200℃时生成CuO,结合原子守恒书写化学方程式;
C.X气体是用于抑制CuCl2水解;
D.CuC1在酸性条件下不稳定,易生成金属铜和Cu2+。
A.制备CuC1时产生的Cl2可以转化为HCl,回收循环利用,Cl2在饱和NaC1溶液中的溶解度小,不能被吸收除去,故A错误;
B.Cu2(OH)2Cl2加热至200℃时生成CuO,结合原子守恒可知,还生成HCl,则化学方程式为:Cu2(OH)2Cl2![]() 2CuO+2HCl↑,故B正确;
2CuO+2HCl↑,故B正确;
C.CuCl2水解生成氢氧化铜和HCl,X气体是用于抑制CuCl2水解,则X为HCl,不是氮气,故C错误;
D.CuC1在酸性条件下不稳定,易生成金属铜和Cu2+,故D错误。
故选B。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目