题目内容
19.在一个1L密闭容器中加入2mol A和1mol B,发生反应:2A(g)+B(g)?3C(g)+D(s).达到平衡时,C的浓度为1.2mol/L,C的体积分数是K,若维持容器的温度和体积不变,投料情况为0.5mol A+0.25mol B+3mol C+a mol D,达平衡后C的体积分数仍是K,则a的取值范围是a≥0.6mol.分析 在恒温恒容条件下,C的浓度仍为1.2mol/L,即平衡时C的物质的量为1.2mol,假设反应完全逆向,则在折算之后要满足n(A)=2mol,n(B)=1mol,D为固体,对平衡移动没有影响,据此分析.
解答 解:在恒温恒容条件下,C的浓度仍为1.2mol/L,即平衡时C的物质的量为1.2mol,假设反应完全逆向,则在折算之后要满足n(A)=2mol,n(B)=1mol,所以投料情况为0.5mol A+0.25mol B+3mol C+a mol D,但又D为固体,对平衡移动没有影响,所以D只要能够与C反应达到平衡状态的量即可,所以D最少为$\frac{3-1.2}{3}$=0.6mol,所以a的取值范围是a≥0.6mol;
故答案为:a≥0.6mol.
点评 本题考查化学平衡的有关计算、等效平衡,难度中等,构建平衡建立的途径是解题关键,注意等效平衡规律:
1、恒温恒压下,按化学计量数转化到一边,满足对应物质的物质的量之比相同,为等效平衡;
2、恒温恒容下,若反应前后气体气体发生变化,按化学计量数转化到一边,满足对应物质的物质的量相等,为等效平衡;若反应前后气体的体积不变,按化学计量数转化到一边,满足对应物质的物质的量之比相同,为等效平衡.

练习册系列答案
相关题目
9.依据图判断,下列说法正确的是( )
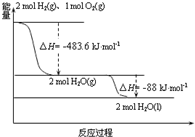

| A. | 氢气的燃烧热为△H=-241.8 kJmol-1 | |
| B. | H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量 | |
| C. | H2O(l)分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g)△H=+571.6 kJ•mol-1 | |
| D. | 2 mol H2(g)与1 mol O2(g)所具有的总能量比 2 mol H2O(g)所具有的总能量低 |
10.电解硫酸铜溶液一段时间后,停止电解.往溶液中加入1mol Cu(OH)2和3mol水,可以使溶液恢复到电解前的成分和浓度,则在电解过程中,电子转移( )mol.
| A. | 10 | B. | 6 | ||
| C. | 2 | D. | 不可能出现此情况 |
7.可逆反应2SO2+O2?2SO3的平衡状态下,保持恒温恒容向容器中加入一定量的O2,下列关于平衡体系的说法正确的是( )(K为平衡常数,S为熵值)
| A. | S不变,K变大,O2转化率增大 | B. | S不变,K变大,SO2转化率减小 | ||
| C. | S变小,K不变,O2转化率减小 | D. | S增大,K不变,SO2转化率增大 |
14.0.1mol/L NH4Cl溶液中,由于NH4+的水解,使得c (NH4+)<0.1mol/L.如果要使c (NH4+)更接近于0.1mol/L,可采取的措施是( )
| A. | 加入少量氢氧化钠 | B. | 加入少量盐酸 | ||
| C. | 加入少量水 | D. | 加热 |
4.升高温度,下列数据不一定增大的是( )
| A. | 某放热反应的正反应速率 | B. | 化学反应的平衡常数 | ||
| C. | 水的离子积 | D. | 吸热反应中反应物的转化率 |
11.下列各组离子能在溶液中大量共存,且溶液呈碱性、透明的是( )
| A. | AlO2-、K+、CO32-、Na+ | B. | Na+、OH-、H2PO4-、NO3- | ||
| C. | Al3+、Cl-、CO32-、Na+ | D. | Fe2+、K+、H+、NO3- |
9.醋酸的下列性质中,可以证明它是弱电解质的是( )
| A. | 1mol•L-1的醋酸溶液中c(H+)=0.01mol•L-1 | |
| B. | 醋酸以任意比与H2O互溶 | |
| C. | 10mL 1mol•L-1的醋酸溶液恰好与10mL 1mol•L-1的NaOH溶液完全反应 | |
| D. | 醋酸溶液的导电性比盐酸弱 |