题目内容
【题目】将溶液(或气体)Y逐滴加入(或通入)一定量的溶液X中(下表),产生沉淀的物质的量(用纵坐标表示)与加入Y物质的量(用横坐标表示)的关系如图所示,则符合图中所示关系的一组物质是

A | B | C | D | |
X |
|
|
|
|
Y |
|
| NaOH | HCl |
A.AB.BC.CD.D
【答案】D
【解析】
由图像可知,将溶液(或气体)Y逐滴加入(或通入)一定量的溶液X中时,先生成沉淀,后沉淀逐渐溶解,且生成沉淀消耗Y的物质的量与溶解沉淀消耗Y的物质的量之比为1:3,据此解答。
由图像可知,将溶液(或气体)Y逐滴加入(或通入)一定量的溶液X中时,先生成沉淀,后沉淀逐渐溶解,且生成沉淀消耗Y的物质的量与溶解沉淀消耗Y的物质的量之比为1:3,
A. 硫酸铝与氯化钡反应的化学方程式为:![]() ,加入过量氯化钡生成的硫酸钡沉淀不会溶解,A项错误;
,加入过量氯化钡生成的硫酸钡沉淀不会溶解,A项错误;
B. 氢氧化钙和二氧化碳反应生成碳酸钙的化学方程式为:![]() ,继续通入
,继续通入![]() ,反应的化学方程式为:
,反应的化学方程式为:![]() ,反应过程中生成沉淀消耗的
,反应过程中生成沉淀消耗的![]() 和沉淀溶解消耗的
和沉淀溶解消耗的![]() 物质的量之比为1:1,与图中所示关系不符,B项错误;
物质的量之比为1:1,与图中所示关系不符,B项错误;
C. 氯化铝和氢氧化钠反应生成氢氧化铝的离子方程式为:![]() ,氢氧化铝和氢氧化钠反应的离子方程式为
,氢氧化铝和氢氧化钠反应的离子方程式为![]() ,反应过程中生成沉淀消耗的氢氧化钠和沉淀溶解消耗的氢氧化钠物质的量之比为3:1,与图中所示关系不符,C项错误;
,反应过程中生成沉淀消耗的氢氧化钠和沉淀溶解消耗的氢氧化钠物质的量之比为3:1,与图中所示关系不符,C项错误;
D. 偏铝酸钠和盐酸反应生成氢氧化铝的离子方程式为:![]() ,氢氧化铝和盐酸反应的离子方程式为:
,氢氧化铝和盐酸反应的离子方程式为:![]() ,反应过程中生成沉淀消耗的盐酸和沉淀溶解消耗的盐酸物质的量之比为1:3,符合图中所示关系,D项正确。
,反应过程中生成沉淀消耗的盐酸和沉淀溶解消耗的盐酸物质的量之比为1:3,符合图中所示关系,D项正确。
答案选D。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案【题目】氮的化合物既是一种资源,也会给环境造成危害。
I.氨气是一种重要的化工原料。
(1)NH3与CO2在120°C,催化剂作用下反应生成尿素:CO2(g)+2NH3(g)![]() (NH2)2CO(s)+H2O(g),ΔH= -x KJ/mol (x>0),其他相关数据如表:
(NH2)2CO(s)+H2O(g),ΔH= -x KJ/mol (x>0),其他相关数据如表:
物质 | NH3(g) | CO2(g) | CO(NH2)2(s) | H2O(g) |
1mol分子中的化学键断裂时需要吸收的能量/KJ | a | b | z | d |
则表中z(用x a b d表示)的大小为________。
(2)120℃时,在2L密闭反应容器中充入3mol CO2与NH3的混合气体,混合气体中NH3的体积分数随反应时间变化关系如图所示,该反应到达平衡时CO2的平均反应速率为_____, 此温度时的平衡常数为_____。

下列能使正反应的化学反应速率加快的措施有___________.
① 及时分离出尿素 ② 升高温度 ③ 向密闭定容容器中再充入CO2 ④ 降低温度
Ⅱ.氮的氧化物会污染环境。目前,硝酸厂尾气治理可采用NH3与于NO在催化剂存在的条件下作用,将污染物转化为无污染的物质。某研究小组拟验证NO能被氨气还原并计算其转化率(已知浓硫酸在常温下不氧化NO气体)。

(l)写出装置⑤中反应的化学方程式_________。
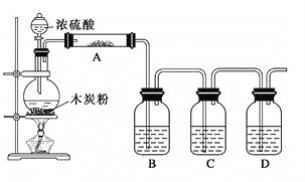
(2)装置①和装置②如下图,仪器A的名称为_____,其中盛放的药品名称为_______。

装置②中,先在试管中加入2-3 粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,加入石灰石的作用是________。
(3)装置⑥中,小段玻璃管的作用是______;装置⑦的作用是除去NO, NO与FeSO4溶液反应形成棕色[Fe(NO)]SO4溶液,同时装置⑦还用来检验氨气是否除尽,若氨气未除尽,可观察到的实验现象是_________。
【题目】无机化合物可根据其组成和性质进行分类。
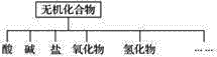
(1)上图所示的物质分类方法名称是____________。
(2)以钠、钾、氢、氧、碳、硫、氮中任两种或三种元素组成合适的物质,分别填在下表中的横线上:
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ②____ | ③____ ④Ba(OH)2 | ⑤Na2CO3 ⑥____ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(3)写出⑦转化为⑤的化学方程式__________。
(4)写出实验室由⑩制备氧气的化学方程式______。
(5)实验室制备⑦常用________和________反应,检验该气体的方法是________。