题目内容
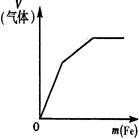
(5分)已知一定物质的量浓度的稀硫酸溶液100mL与足量的铁粉充分反应,生成4.48L氢气(标准状况下)。求
⑴有多少克铁参加反应
⑵该稀硫酸的物质的量浓度
⑴有多少克铁参加反应
⑵该稀硫酸的物质的量浓度
(5分)
n(H2)=4.48L/(22.4L/mol)=0.2mol
n(Fe)= n(H2)= 0.2mol
mFe)=0.2mol×(56g/mol)=11.2g
n(H2SO4) = n(H2)= 0.2mol
c(H2SO4) = 0.2mol/(0.1L)=2mol/L
n(H2)=4.48L/(22.4L/mol)=0.2mol
n(Fe)= n(H2)= 0.2mol
mFe)=0.2mol×(56g/mol)=11.2g
n(H2SO4) = n(H2)= 0.2mol
c(H2SO4) = 0.2mol/(0.1L)=2mol/L
略

练习册系列答案
相关题目
 石膏(CaSO4·2H2O)的生产流程示意图:
石膏(CaSO4·2H2O)的生产流程示意图: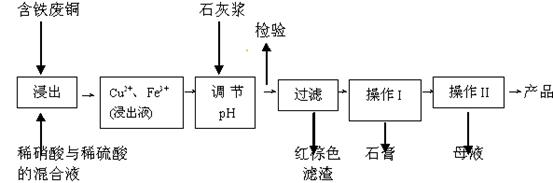
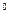 C)
C)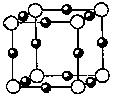
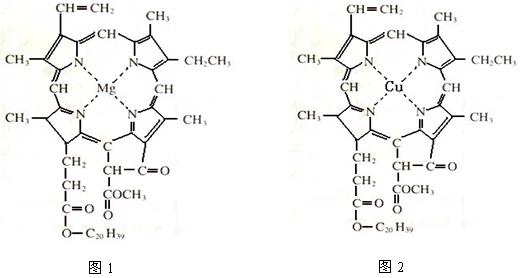
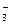 、Cl-、Al3+
、Cl-、Al3+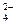 、NO
、NO