题目内容
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
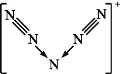
A. 0.5mol![]() 含中子数为8NA
含中子数为8NA
B. 常温下,1 mol NH4Cl含共价键数目为5NA
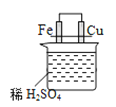
C. 足量的Cu与含溶质1mol的浓H2SO4反应,转移的电子数为NA
D. 11.2LH2和O2的混合气体中分子数目为0.5NA
【答案】A
【解析】
A.![]() 质子数16,中子数是16,所以0.5mol
质子数16,中子数是16,所以0.5mol![]() 含中子数为8NA,故A正确;B.1molNH4Cl含N-H共价键4mol,所以1molNH4Cl含共价键数目为4NA,故B错误;C.足量的Cu与含溶质1mol的浓H2SO4反应,由于随反应进行,硫酸浓度减小,稀硫酸和铜不反应,所以足量的Cu与含溶质1mol的浓H2SO4反应转移的电子数小于NA,故C错误;D. 11.2LH2和O2的混合气体,没指明状态,无法计算物质的量,故D错误;答案为A。
含中子数为8NA,故A正确;B.1molNH4Cl含N-H共价键4mol,所以1molNH4Cl含共价键数目为4NA,故B错误;C.足量的Cu与含溶质1mol的浓H2SO4反应,由于随反应进行,硫酸浓度减小,稀硫酸和铜不反应,所以足量的Cu与含溶质1mol的浓H2SO4反应转移的电子数小于NA,故C错误;D. 11.2LH2和O2的混合气体,没指明状态,无法计算物质的量,故D错误;答案为A。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案【题目】Ⅰ.人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
(配制KMnO4标准溶液)
如图所示是配制50 mL KMnO4标准溶液的过程示意图。

(1)请你观察图示判断,其中不正确的操作有__________ (填序号)。
(2)其中确定50 mL溶液体积的容器是________(填名称)。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将________(填“偏大”或“偏小”)。
(测定血液样品中Ca2+的浓度)
抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol·L-1 KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)配平草酸与KMnO4反应的离子方程式:__MnO+ H2C2O4+ H+=== Mn2++ CO2↑+ H2O。
(5)滴定终点时的现象是_____________________________________
(6)经过计算,血液样品中Ca2+的浓度为__________m mol·cm-3。
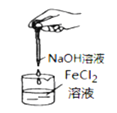
Ⅱ. 某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。
实验1试剂:酸化的0.5 mol·L-1FeSO4溶液(pH = 0.2),5% H2O2溶液(pH = 5)。
操作 | 现象 |
取2 mL上述FeSO4溶液于试管中,加入5滴5% H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡。测得反应后溶液pH=0.9 |
向反应后的溶液中加入KSCN溶液 | 溶液变红 |
(1)H2O2的电子式是_______,上述实验中H2O2溶液与FeSO4溶液反应的离子方程式是_________。
(2)产生气泡的原因是____________________________________________。