题目内容
12.科学家最近在-100℃的低温下合成了一种键线式为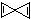 的烃X,根据分析,下列说法中不正确的是( )
的烃X,根据分析,下列说法中不正确的是( )| A. | X的分子式为C5H4 | |
| B. | 分子中氢原子的化学环境只有一种 | |
| C. | 1 mol X在一定条件下可与2 mol氢气发生反应 | |
| D. | X不能使高锰酸钾酸性溶液褪色 |
分析 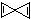 中含5个C、4个H,分子中含碳碳双键,结合烯烃的性质来解答.
中含5个C、4个H,分子中含碳碳双键,结合烯烃的性质来解答.
解答 解:A.由结构简式可知分子式为C5H4,故A正确;
B.分子结构对称,只含有1种H原子,故B正确;
C.含2个C=C,C=C与氢气以1:1加成,1molX在一定条件下可与2mol氢气发生反应,故C正确;
D.含C=C,能使酸性高锰酸钾溶液褪色,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃性质的考查,注意选项B中含1种位置的H,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.针对节能减排,某化学学习研究性小组提出如下方案,你认为不够科学合理的是( )
| A. | 采用电解水法制取无污染的氢能 | B. | 完善煤液化制取汽油的技术 | ||
| C. | 研制推广以甲醇为燃料的汽车 | D. | 进一步提高石油加工工艺 |
4.95%的乙醇(密度为0.78g/cm3)用等体积的蒸馏水稀释后,所得溶液中乙醇的质量分数约为( )
| A. | 42% | B. | 48% | C. | 51% | D. | 65% |
1.氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A. | 两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 | |
| B. | NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 | |
| C. | NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 | |
| D. | 氨气的相对分子质量大于甲烷 |

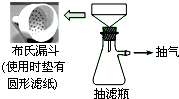 卷心菜中含有丰富的维生素C,维生素C在酸性溶液中能被碘氧化.某实验小组通过如下实验对卷心菜中维生素C的含量进行测定.
卷心菜中含有丰富的维生素C,维生素C在酸性溶液中能被碘氧化.某实验小组通过如下实验对卷心菜中维生素C的含量进行测定.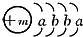 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.