题目内容
2.有A、B、C、D、E五种短周期元素,它们的原子序数依次增大. 已知A和B原子具有相同的电子层数,且A的最外层电子数是次外层电子数的两倍,C是该周期中原子半径最大的元素,C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,E与D相邻. 试根据以上叙述回答:(1)元素名称:A碳 C钠 E氯
(2)写出AB2与过量氢氧化钠溶液反应的离子方程式CO2+2OH-=CO32-+H2O写出 C2B2与AB2反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2↑;
(3)画出D的原子结构示意图
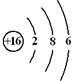 用电子式表示化合物 C2D 的形成过程
用电子式表示化合物 C2D 的形成过程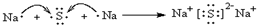
(4)E在元素周期表中的位置第三周期第ⅤⅡA族.
分析 A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A的最外层电子数是次外层电子数的两倍,最外层电子数不超过8个,K层不超过2个,则A原子次外层为K层,则A是C元素;A和B原子具有相同的电子层数,则B为第二周期元素;
C是该周期中原子半径最大的元素,且C原子序数大于B,所以C为第三周期元素,为Na元素;
C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,该化合物为过氧化钠,则B单质是氧气,B为O元素,D是S元素,E与D相邻,且原子序数大于D,所以E是Cl元素,再结合原子结构、物质结构和性质解答.
解答 解:A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A的最外层电子数是次外层电子数的两倍,最外层电子数不超过8个,K层不超过2个,则A原子次外层为K层,则A是C元素;A和B原子具有相同的电子层数,则B为第二周期元素;
C是该周期中原子半径最大的元素,且C原子序数大于B,所以C为第三周期元素,为Na元素;
C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,则B单质是氧气,B为O元素,D是S元素,E与D相邻,且原子序数大于D,所以E是Cl元素,
(1)通过以上分析知,A、C、E分别是碳、钠、氯元素,
故答案为:碳;钠;氯;
(2)A是C元素、B是O元素,CO2与过量氢氧化钠溶液反应生成碳酸钠和水,离子方程式为CO2+2OH-=CO32-+H2O,Na2O2与CO2发生反应生成碳酸钠和氧气,反应方程式为,
故答案为:CO2+2OH-=CO32-+H2O;2Na2O2+2CO2=2Na2CO3+O2↑;
(3)D是S元素,其原子核外有3个电子层、最外层有6个电子,其原子结构示意图为 ;Na2S为离子化合物,用电子式表示硫化钠的形成过程为:
;Na2S为离子化合物,用电子式表示硫化钠的形成过程为: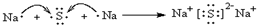 ,
,
故答案为: ;
;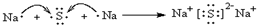 ;
;
(4)E为Cl元素,原子序数为17,最外层含有7个电子,氯元素在周期表中第三周期第ⅤⅡA族,
故答案为:第三周期第ⅤⅡA族.
点评 本题考查位置结构性质的相互关系及应用,题目难度中等,试题涉及原子结构、物质结构和物质性质,侧重考查学生对元素化合物知识的掌握、元素的推断,难点是用电子式表示Na2S的形成过程.

| A. | 一氧化碳 | B. | 二氧化硫 | C. | 二氧化碳 | D. | PM2.5 |
| A. | 由非电解质溶于水得到的溶液 | |
| B. | c(H+)、c(OH-)均为5.0×10-7mol•L-1的溶液 | |
| C. | 等物质的量的强酸与强碱反应得到的溶液 | |
| D. | 将pH=9的烧碱溶液稀释100倍所得到的溶液 |
| A. | 原子半径X>Y>Z | B. | 稳定性HX>H2Y>ZH3 | ||
| C. | 非金属性X>Y>Z | D. | 阴离子的还原性Z3->Y2->X- |
| A. | X与Y形成化合物时,X可以显负价,Y显正价 | |
| B. | 气态氢化物的稳定性:HmY小于HnX | |
| C. | 第一电离能可能Y小于X | |
| D. | 最高价含氧酸的酸性:X对应的酸的酸性弱于Y对应的酸的酸性 |
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 2.0X10-10 | 5.4X10-13 | 8.3X10-17 | 2.0X10-41 | 2.0X10-12 |
| A. | 20℃时.AgCl饱和溶液和Ag2CrO4饱和溶液中.Ag+物质的量浓度由大到小的顺序是Ag2CrO4>AgCl | |
| B. | 20℃时,向相同浓度的KCl和KBr混合溶液中逐滴滴加AgNO3溶液.会先生成浅黄色沉淀 | |
| C. | 20℃时,向相同浓度的KCl和KBr混合溶液中逐滴滴加AgNO3溶液,当两种沉淀共存时.c(Br-):C(C1-)=2.7×10-3 | |
| D. | 在100ml AgCl、AgBr、AgI饱和的混合溶液中加入足量浓AgNO3溶液,产生沉淀AgI质量最多 |
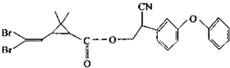 拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )| A. | 属于芳香烃 | B. | 属于有机化合物 | ||
| C. | 不能发生取代反应 | D. | 在一定条件下可以发生加成反应 |
| A. | 镁与盐酸反应放出氢气 | B. | 碳酸钙高温分解 | ||
| C. | 硫在空气或氧气中燃烧 | D. | Ba(OH)2•8H2O与NH4Cl反应 |
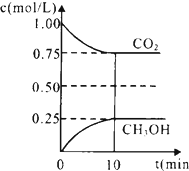 二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.
二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.