题目内容
17. 内酯类化合物在药物、涂料等应用广泛.
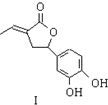
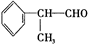
内酯类化合物在药物、涂料等应用广泛.(1)下列化合物I的说法,正确的是AC.
A.遇FeCl3溶液可显紫色
B.可发生加成反应和银镜反应
C.能使酸性KMnO4、Br2的CCl4溶液褪色
D.1mol化合物I最多能与2molNaOH反应
(2)已知:反应
①:
 +$\frac{1}{2}$O2+CO2$\stackrel{催化剂}{→}$
+$\frac{1}{2}$O2+CO2$\stackrel{催化剂}{→}$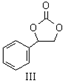
反应②:CH3CH2NH2+CO2+
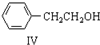 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$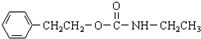 +H2O
+H2O化合物II的分子式为C8H8,1mol化合物II能与4molH2恰好完全反应生成饱和烃类化合物.
(3)化合物IV可由芳香族化合物V与H2加成反应获得,且V不能发生酯化反应,V的结构简式为
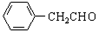 ;由IV生成II的反应条件为浓硫酸、加热.
;由IV生成II的反应条件为浓硫酸、加热.(4)芳香族化合物VI是Ⅲ的一种同分异构体,VI分子中含有两种官能团,不能发生银镜反应,但能通过加成反应使溴的CCl4溶液褪色,VI的结构简式是
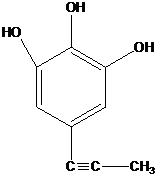 .
.(5)利用类似反应②的方法,仅以BrCH2CH2-NH2为有机原料合成
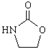 ,涉及的反应方程式为BrCH2CH2-NH2+NaOH$→_{△}^{H_{2}O}$HOCH2CH2NH2、HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$
,涉及的反应方程式为BrCH2CH2-NH2+NaOH$→_{△}^{H_{2}O}$HOCH2CH2NH2、HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$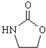 +H2O.
+H2O.
分析 (1)A.酚能和氯化铁溶液发生显色反应;
B.羟基或羧基能发生酯化反应,醛基能发生银镜反应;
C.含碳碳双键可发生加成、氧化反应;
D.能和NaOH反应的为酚羟基、羧基;
(2)Ⅱ中含有9个C原子、10个H原子,据此确定化学式;能和氢气发生加成反应的有苯环和碳碳双键;
(3)化合物IV中含醇-OH,可由芳香族化合物V与H2加成反应获得,且V不能发生酯化反应,则V为醛;IV生成II,-OH转化为碳碳双键;
(4)VI是Ⅲ的一种同分异构体,VI分子中含有两种官能团,不能发生银镜反应,但能通过加成反应使溴的CCl4溶液褪色,含酚-OH、碳碳三键;
(5)由反应②CH3CH2NH2+CO2+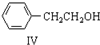 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$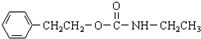 +H2O,仅以BrCH2CH2-NH2为有机原料合成
+H2O,仅以BrCH2CH2-NH2为有机原料合成 ,先发生水解反应生成OHCH2CH2-NH2,再与二氧化碳发生信息②的反应即可.
,先发生水解反应生成OHCH2CH2-NH2,再与二氧化碳发生信息②的反应即可.
解答 解:(1)A.含酚-OH,能和氯化铁溶液发生显色反应,故A正确;
B.苯环与双键均可发生加成反应,该物质不含醛基,所以不能发生银镜反应,故B错误;
C.含碳碳双键能和溴发生加成反应,与高锰酸钾发生氧化反应,能使酸性KMnO4、Br2的CCl4溶液褪色,故C正确;
D.能和NaOH反应的为酚羟基、羧基,1mol化合物I最多能与3mol NaOH反应,故D错误;
故选AC;
(2)Ⅱ中含有8个C原子、8个H原子,其化学式为C8H8;能和氢气发生加成反应的有苯环和碳碳双键,1mol化合物Ⅱ能与4mol H2恰好完全反应生成饱和烃类化合物,
故答案为:C8H8;4;
(3)化合物IV中含醇-OH,可由芳香族化合物V与H2加成反应获得,且V不能发生酯化反应,则V为醛,则V的结构简式为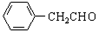 ;IV生成II,-OH转化为碳碳双键,为醇的消去反应,其反应条件是浓硫酸、加热,
;IV生成II,-OH转化为碳碳双键,为醇的消去反应,其反应条件是浓硫酸、加热,
故答案为: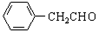 ;浓硫酸、加热;
;浓硫酸、加热;
(4)VI是Ⅲ的一种同分异构体,VI分子中含有两种官能团,不能发生银镜反应,但能通过加成反应使溴的CCl4溶液褪色,含酚-OH、碳碳三键,其结构简式为 ,故答案为:
,故答案为: ;
;
(5)仅以BrCH2CH2-NH2为有机原料合成 ,发生BrCH2CH2-NH2+NaOH$→_{△}^{H_{2}O}$HOCH2CH2NH2、HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$
,发生BrCH2CH2-NH2+NaOH$→_{△}^{H_{2}O}$HOCH2CH2NH2、HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$ +H2O,
+H2O,
故答案为:BrCH2CH2-NH2+NaOH$→_{△}^{H_{2}O}$HOCH2CH2NH2;HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$ +H2O.
+H2O.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力、推断能力的综合考查,(5)为解答的难点,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | 二氧化碳和环氧丙烷在催化剂作用下可生成一种可降解的高聚物 | |
| B. | 化石燃料的燃烧和含硫金属矿石的冶炼等都是造成SO2污染的重要原因 | |
| C. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| D. | 氟氯烃的大量使用会破坏臭氧层,火箭、导弹将大量废气排放到高空,也会加速臭氧分解 |
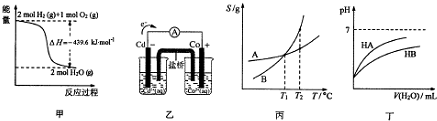
| A. | 由甲推知氢气的燃烧热为219.8kJ•mol-1 | |
| B. | 由乙推知离子反应Co2+(ap)+Cd(s)═Co(s)+Cd2+(ap)可以发生 | |
| C. | 由丙可知:将A、B饱和溶液分别由T1℃升温T2℃时,溶质的质量分数:B>A | |
| D. | 由丁可知:同温度、同浓度NaA溶液与NaB溶液相比,其pH:NaA>NaB |
| 选项 | 事实 | 化学方程式 |
| A | 常温下,可用铝制容器盛放浓硝酸 | A l+3HNO3(浓)=Al(OH)3+3NO2↑ |
| B | 可用生石灰做工业废气脱硫酸 | 2CaO+2SO2+O2=2CaSO4 |
| C | 电解MgCl2溶液冶炼Mg | MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ |
| D | 侯德榜用饱和食盐水、氨水、CO2制备纯碱 | 2NaCl+2NH3+CO2+H2O=2NH4Cl+NaCO3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 1L 1 mol•L-1盐酸中含有nA个HCl分子 | |
| B. | 32g O2与O3的混合物含有2nA个氧原子 | |
| C. | 1L 1 mol•L-1CuCl2溶液中含有nA个Cu2+ | |
| D. | 1mol Na与足量Cl2反应,转移2nA个电子 |
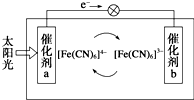 一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是( )
一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是( )| A. | K+移向催化剂b | |
| B. | 催化剂a表面发生的化学反应:[Fe(CN)6]4--e-═[Fe(CN)6]3- | |
| C. | Fe(CN)63-在催化剂b表面被氧化 | |
| D. | 电解池溶液中的[Fe(CN)6]4-和[Fe(CN)6]3-浓度基本保持不变 |
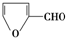

 )是一种重要的化工原料,其合成路线如下:
)是一种重要的化工原料,其合成路线如下: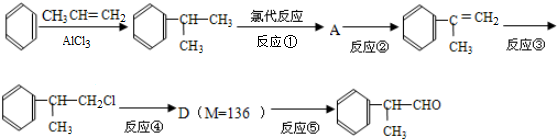
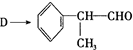 反应的化学方程式为2
反应的化学方程式为2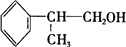 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2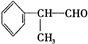 +2H2O.
+2H2O.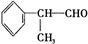 +2[Ag(NH3)2]OH$\stackrel{△}{→}$
+2[Ag(NH3)2]OH$\stackrel{△}{→}$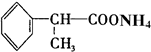 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.