题目内容
【题目】图1是铜锌原电池示意图,图2中,x轴表示实验时流入正极的电子的物质的量, 下列说法中不正确的是
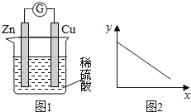
A.y轴可表示锌片的质量
B.y轴可表示溶液中c(H+)
C.若导线上转移2mol电子,则有2molH2生成
D.溶液中的阳离子向正极移动,阴离子向负极移动
【答案】C
【解析】
锌-铜-硫酸构成的原电池中,根据原电池原理,锌片作负极,随着反应的进行,锌单质失去电子生成锌离子进入溶液,锌片的质量会不断减轻;铜作正极,硫酸溶液中的氢离子在铜电极上放电生成氢气,溶液中的氢离子浓度会减小;溶液中阳离子移向正极,阴离子移向负极。
A.由图像,结合分析可知,随着反应的进行,电路中转移的电子数增多,锌片会不断溶解,质量减轻,故A正确;
B.由分析可知,溶液中氢离子浓度随着转移的电子数增多而减小,故B正确;
C.根据化合价变化,每生成1mol氢气,电路中转移的电子数为2mol,则若导线上转移2mol电子,则有1molH2生成,故C错误;
D.原电池装置中,溶液中阳离子移向正极,阴离子移向负极,故D正确;
综上所述,答案为C。

练习册系列答案
相关题目







