题目内容
请根据表中化学键的键能计算反应SiCl4(g)+2H2(g)═Si(s)+4HCl(g)的反应热△H为( )
| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
| 键能/KJ?mol-1 | 360 | 436 | 431 | 176 |
| A、240 | B、412 |
| C、236 | D、667 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:化学反应方程式中的反应热=反应物的键能之和-生成物的键能之和.
解答:
解:△H=360kJ/mol×4+436kJ/mol×2-176kJ/mol×2-431kJ/mol×4=+236 kJ/mol.
故选:C.
故选:C.
点评:本题考查了反应热的计算,注意反应热中硅的键能,在硅晶体中每个硅原子和其它4个硅原子形成4个共价键,每个Si-Si键被两个Si原子共用,所以每个硅原子含有2个共价键,此点为易错点.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
下列关于有机物的叙述正确的是( )
| A、汽油、柴油和植物油的成分都是碳氢化合物 |
| B、棉花和合成纤维的主要成分均为纤维素 |
| C、乙烯和苯蒸气都能使溴水褪色,不能鉴别乙烯和苯蒸气 |
| D、甲烷跟氯气在光照条件下的反应与乙酸、乙醇和浓硫酸共热时的反应类型相同 |
下列选项中的离子方程式书写正确的是( )
| A、稀硫酸和Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B、过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O |
| C、铜在加热条件下与浓硫酸反应:Cu+SO42-+4H+═Cu2++SO2↑+2H2O |
| D、SO2使溴水褪色:SO2+Br2+2H2O═SO42-+2Br-+4H+ |
将如图所示实验装置的K闭合,下列判断正确的是( )
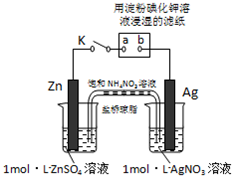

| A、Ag电极上发生氧化反应 |
| B、盐桥中NO3-向Zn电极移动 |
| C、电子沿Zn→a→b→Ag路径流动 |
| D、片刻后可观察到滤纸a点变蓝 |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍也是Y原子最外层电子数的3倍.下列说法正确的是( )
| A、Y与Z形成的简单离子核外电子排布相同 |
| B、X的氧化物为离子化合物 |
| C、Z的氢化物的水溶液在空气中容易变质 |
| D、X与Z对应的氧化物的水化物一定为强酸 |
将质量为w1 g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1 L.向溶液中逐渐加入浓度为a mol/L的HCl溶液,反应过程中先有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2 L.将溶液蒸干灼烧得固体w2 g.下列关系式中正确的是( )
A、n(Na)+3n(Al)=
| ||
B、aV2=
| ||
| C、35.5aV2=w2-w1 | ||
| D、35.5aV2>(w2-w1) |
 如图为一种广泛使用的高分子材料助剂的结构简式,下列说法正确的是(CH3CH2CH2CH3可表示为
如图为一种广泛使用的高分子材料助剂的结构简式,下列说法正确的是(CH3CH2CH2CH3可表示为 )( )
)( )| A、该有机物的分子式为C24H40O4 |
| B、1mol该有机物与氢气发生加成反应,最多消耗5mol氢气 |
| C、该有机物在氢氧化钠作用下发生水解反应得到三种有机物 |
| D、该有机物在FeBr3存在下与液溴发生取代反应生成两种一溴代物 |
