题目内容
【题目】阅读下列实验内容,根据题目要求回答问题。
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol·L-1的NaOH溶液滴定上述稀H2SO4溶液25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14mol·L-1 NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入几滴酚酞做指示剂
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管,调整液面,记下开始读数
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作一次
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
滴定操作的正确顺序是(用序号填写)_______________。
(2)在D操作中应该调整液面到_________________,并使尖嘴处_____________。
(3)配制准确浓度的稀H2SO4溶液,必须使用的主要容器是__________________。
(4)滴定到终点时锥形瓶内溶液的pH约为________;终点时颜色变化是____________。
(5)用标准NaOH溶液滴定时,应将标准NaOH溶液注入____(选填“甲”或“乙”)中。
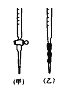
(6)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值___________(选填“偏大”“偏小”或“无影响”)。
(7)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果到小数点后二位)____。
【答案】ECDBAGF或ECBADGF 0刻度或0刻度一下某一具体位置 充满标准NaOH溶液 100mL容量瓶 9 无色变为浅红色(或粉红色),且半分钟内不褪色 乙 偏小 8.40mol/L
【解析】
(1)滴定的操作步骤为:验漏→水洗→润洗→装液→读数→滴定→读数→计算;故正确的操作顺序为ECDBAGF或ECBADGF;
(2)装液之后,读数前应将液面调至0刻线或0刻线以下,并使尖嘴处充满溶液,若尖嘴处有气泡,则需要将气泡排出;
(3)题中说明需要配置100mL稀H2SO4溶液,故需要使用100mL容量瓶来配制;
(4)滴定终点是溶液由无色变为浅红色,且30s内不变色,此时溶液的pH约为9(酚酞的变色范围为8.2-10.0);
(5)NaOH应装入乙(碱式滴定管)中;
(6)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,会使得V(碱)偏小,根据c(酸)×V(酸)= c(碱)×V(碱)可得知,c(酸)偏小;
(7)25.00mL H2SO4中,n(H2SO4)=c(NaOH)×V(NaOH)=0.14molL-1×15.00×10-3L=0.0021mol,则100mL H2SO4中,n(H2SO4)=![]() ×0.0021mol=0.0084mol,故1mL H2SO4的浓度为
×0.0021mol=0.0084mol,故1mL H2SO4的浓度为![]() =8.40mol/L。
=8.40mol/L。

【题目】下列有关水溶液中的平衡相关的问题,请填空
(1)已知常温下,将氯化铝溶液和碳酸钠溶液混合,有白色沉淀产生,写出反应离子方程式______________
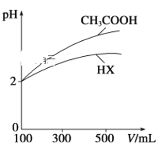
(2)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示。同浓度,同体积的CH3COONa与NaX溶液,离子总数目: CH3COONa溶液_______NaX溶液(填>,<,=)
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
①25℃时,浓度均为0.01 mol·L-1 HCN和NaCN混合溶液显_____性(填酸,碱,中)。溶液中HCN浓度_________CN-浓度(填>,<,=)
②25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中![]() =____。
=____。
(4)在25°C下,将x mol·L-1的氨水与y mol·L-1的盐酸等体积混合,反应后溶液中显中性,则c(NH4+)____c(Cl-)(填“>” 、“<” 或“=” );用含x和y的代数式表示出氨水的电离平衡常数______。
【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
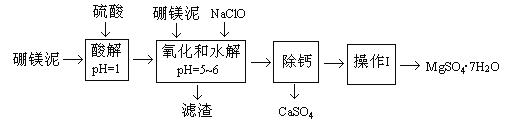
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有_________。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有_________。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式_________。在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为________________。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法_________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤_________、_________。
(6)如果提供的硼镁泥共100 g,得到的MgSO4·7H2O 196.8 g,则MgSO4·7H2O的产率为_________。