题目内容
(7分)某同学模拟工业“折点加氯法”处理氨氮废水的原理,进行如下研究。
| 装置(气密性良好,试剂已添加) | 操作 | 现象 |
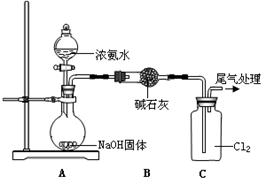 | 打开分液漏斗活塞,逐滴加入浓氨水 | ⅰ.C中气体颜色变浅 ⅱ.稍后,C中出现白烟并逐渐增多 |
(1)浓氨水分解可以制氨气,写出A中反应的化学方程式是 。从平衡移动 的角度分析NaOH固体在氨水分解中的作用 。
(2)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)= N2(g)+6HCl(g) ?H=—456 kJ·mol-1
已知:
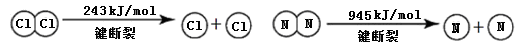
①NH3的电子式是 。
②断开1mol H-N键与断开1molH-Cl键所需能量相差约为 ,
(3)现象ⅱ中产生白烟的化学方程式是 。
(4)为避免生成白烟,该学生设计了下图装置以完成Cl2和NH3的反应。
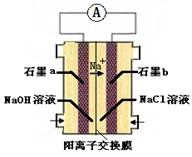
若该装置能实现设计目标,则①石墨b电极上发生的是 反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式: 。
(1)NH3·H2O NH3↑+H2O 氨水分解过程吸热,NaOH固体溶于水放热,使环境温度升高,氨水分解反应平衡正向移动,促进了氨水分解。(或NaOH固体有吸水性,能吸收氨水分解生成的水,促进氨水分解平衡正向移动)
NH3↑+H2O 氨水分解过程吸热,NaOH固体溶于水放热,使环境温度升高,氨水分解反应平衡正向移动,促进了氨水分解。(或NaOH固体有吸水性,能吸收氨水分解生成的水,促进氨水分解平衡正向移动)
(2)①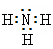 ② 40 (3)HCl+NH3=NH4Cl
② 40 (3)HCl+NH3=NH4Cl
(4)①还原 ;②2NH3+6OH-—6e-=N2+6H2O
解析试题分析:(1)浓氨水加热分解可以制氨气, A中反应的化学方程式是NH3·H2O NH3↑+H2O;氨水分解过程吸热,NaOH固体溶于水放热,使环境温度升高,氨水分解反应平衡正向移动,促进了氨水分解。(2)①NH3的电子式是
NH3↑+H2O;氨水分解过程吸热,NaOH固体溶于水放热,使环境温度升高,氨水分解反应平衡正向移动,促进了氨水分解。(2)①NH3的电子式是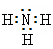 ;②6×N—H+3×243KJ -945KJ -6×H—Cl="—456" kJ,解得N—H与Cl—H的键能的差是40KJ/mol.断开1mol H-N键与断开1molH-Cl键所需能量相差约为40KJ/mol。(3)现象ⅱ中产生白烟NH4Cl的化学方程式是HCl+NH3=NH4Cl。(4)①由图示可知Na+向b电极区域移动,根据同种电荷相互排斥,异种电荷相互吸引的原则,石墨b电极是阴极,在阴极上发生的是还原反应;②石墨a电极是阳极,在阳极上反应氧化反应,该电极的电极反应式:2NH3+6OH-—6e-=N2+6H2O。
;②6×N—H+3×243KJ -945KJ -6×H—Cl="—456" kJ,解得N—H与Cl—H的键能的差是40KJ/mol.断开1mol H-N键与断开1molH-Cl键所需能量相差约为40KJ/mol。(3)现象ⅱ中产生白烟NH4Cl的化学方程式是HCl+NH3=NH4Cl。(4)①由图示可知Na+向b电极区域移动,根据同种电荷相互排斥,异种电荷相互吸引的原则,石墨b电极是阴极,在阴极上发生的是还原反应;②石墨a电极是阳极,在阳极上反应氧化反应,该电极的电极反应式:2NH3+6OH-—6e-=N2+6H2O。
考点:考查氨气的制取方法、物质的电子式、键能大小的比较、化学方程式、电极反应式的书写的知识。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案下列说法正确的是:( )
A.在100 ℃.101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的ΔH ="+" 40.69 kJ·mol-1 H2O(l) 的ΔH ="+" 40.69 kJ·mol-1 |
| B.已知MgCO3的Ksp = 6.82 × 10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+) = c(CO32-),且c(Mg2+) · c(CO32-)= 6.82 × 10-6 |
| C.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的pH减小 |
| D.已知: |
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
则可以计算出反应
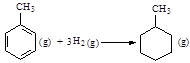 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1 乙醇分子结构中各种化学键如下所示,关于乙醇在各种反应中断键的说明不正确的为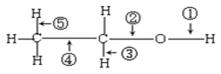
| A.和乙酸共热时,断裂①键 |
| B.和金属钠反应时,键①断裂 |
| C.和P2O5共热时,键②⑤断裂 |
| D.在铜催化下和氧气反应时,键①⑤断裂 |
(16分) 碳及其化合物有广泛的用途。
(1)反应C(s)+ H2O(g) 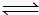 CO(g) +H2(g) ΔH=" +131.3" kJ?mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g) +H2(g) ΔH=" +131.3" kJ?mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
| A.增加碳的用量 | B.升高温度 | C.用CO吸收剂除去CO | D.加入催化剂 |
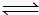 2CO(g) △H=+172.5kJ?mol-1
2CO(g) △H=+172.5kJ?mol-1则反应 CO(g)+H2O(g)
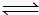 CO2(g)+H2(g) 的△H= kJ?mol-1。
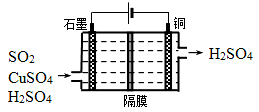
CO2(g)+H2(g) 的△H= kJ?mol-1。(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)
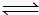 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:| t / min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
②该温度下,此反应的平衡常数K=______ _____;
③其它条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数______(填“增大”、“减小”或“不变”)。
(12分)(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体(分子式为CH4·9H2O),则356g“可燃冰”释放出的甲烷燃烧,生成液态水时能放出1780.6 kJ的热量,则甲烷燃烧的热化学方程式可表示为:_______________________________。
(2) 在100℃时,将0.100mol的N2O4气体充入1 L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到下表数据: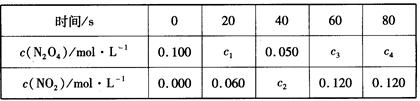
①从表中分析:该反应的平衡常数为___________;
②在上述条件下,60s内N2O4的平均反应速率为_____________;
③达平衡后下列条件的改变可使NO2浓度增大的是_________。
| A.增大容器的容积 | B.再充入一定量的N2O4 |
| C.再充入一定量的NO2 | D.再充入一定量的He |
②用等浓度的盐酸分别中和等体积浓度均为0.01mol/L的氨水和NaOH溶液,消耗盐酸的体积分别为V3、V4,则V3_____V4;
③用等浓度的盐酸分别和等体积浓度均为0.01mol/L的氨水和NaOH溶液反应,最后溶液均为中性,消耗盐酸的体积分别为V5、V6,则V5_____V6。
(14分)合成氨是人类研究的重要课题,目前工业合成氨的原理为:
合成氨是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g) 2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
相持恒温、恒容,测的反应达到平衡时关系数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2mol NH3 |
| 达到平衡的时间/min | | 6 | 8 |
| 平衡时 N2的体积密度 | C1 | 1.5 | |
| 混合气体密度/g·L-1 |  |  | |
| 平衡常数/ L2·mol-2 | K甲 | K乙 | K丙 |
a.容器内H2、N2、NH3的浓度只比为1:3:2 b.容器内压强保持不变
c.
 d.混合气体的密度保持不变
d.混合气体的密度保持不变e.混合气体的平均相对分子质量不变
(2)容器乙中反应从开始到达平衡的反应速度为
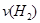 =
= (3)在该温度下甲容器中反应的平衡常数K (用含C1的代数式表示)
(4)分析上表数据,下列关系正确的是 (填序号):
a.
 b.氮气的转化率:
b.氮气的转化率: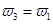 c.
c. 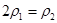 d.
d.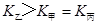
(5)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热△H=-286KJ/mol,则由次原理制NH3反应的热化学方程式为
(6)希腊阿里斯多德大学的George Mamellos和Michacl Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氨气稀释的氮气分别通入一个加热到
 的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。
的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。