题目内容
(14分)合成氨是人类研究的重要课题,目前工业合成氨的原理为:
合成氨是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g) 2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
相持恒温、恒容,测的反应达到平衡时关系数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2mol NH3 |
| 达到平衡的时间/min | | 6 | 8 |
| 平衡时 N2的体积密度 | C1 | 1.5 | |
| 混合气体密度/g·L-1 | 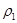 |  | |
| 平衡常数/ L2·mol-2 | K甲 | K乙 | K丙 |
a.容器内H2、N2、NH3的浓度只比为1:3:2 b.容器内压强保持不变
c.
 d.混合气体的密度保持不变
d.混合气体的密度保持不变e.混合气体的平均相对分子质量不变
(2)容器乙中反应从开始到达平衡的反应速度为
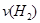 =
= (3)在该温度下甲容器中反应的平衡常数K (用含C1的代数式表示)
(4)分析上表数据,下列关系正确的是 (填序号):
a.
 b.氮气的转化率:
b.氮气的转化率: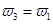 c.
c. 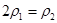 d.
d.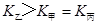
(5)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热△H=-286KJ/mol,则由次原理制NH3反应的热化学方程式为
(6)希腊阿里斯多德大学的George Mamellos和Michacl Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氨气稀释的氮气分别通入一个加热到
 的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。
的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。
(14分,每空2分)(1)be(全对2分,对1个得1分,有错不得分)
(2)0.25mol/(L·min)(单位不写或错写扣1分)
(3)K=4(1-C1)2/C1·(3C1-1.5)3
(4)C
(5)2N2(g)+6H2O(l)="4" NH3(g)+3 O2(g)△H=+1530kJ·mol-1
(6)阴 N2+6H+++6e-==2 NH3
解析试题分析:(1)合成氨反应是反应前后气体物质的量发生变化的可逆反应,所以压强不变时证明已达平衡状态,b正确;容器内的各物质的浓度比符合化学计量数之比时未必是平衡状态,a错误;根据好好的定义,正逆反应速率相等时达平衡状态,氢气的反应速率是氮气反应速率的3倍,c错误;容器的体积不变,所以气体的密度始终不变,d错误;气体的质量不变,而气体的总物质的量变化,当平均相对分子质量不变时已达平衡状态,e正确,答案选be;
(2)根据氮气的体积密度即浓度可计算平衡时氮气的物质的量为3mol,则消耗氮气的物质的量是1mol,氢气的物质的量是3mol,所以用氢气表示的反应速率为3mol/2L/6min="0.25" mol/(L·min);
(3)氮气、氢气的起始浓度分别为1mol/L、1.5mol/L,根据氮气平衡时的浓度可计算消耗氮气的浓度为1- C1,消耗氢气的浓度是3(1- C1),生成氨气的浓度为2(1- C1),根据化学平衡常数的表达式可得K甲=c(NH3)2/c(N2)c(H2)3=4(1-C1)2/C1·(3C1-1.5)3
(4)A、乙容器的反应物浓度是甲容器的2倍,保持恒温、恒容,乙容器相当于在2个甲的基础上又正向移动,氮气的浓度减小,所以2 C1>1.5mol/L,错误;B、把丙的2mol氨气转化为3mol氢气和1mol氮气与丙达到的平衡是等效的。甲与丙相比,甲的氢气浓度大,氮气的转化率高,错误;C、乙容器的气体质量是甲容器的气体质量的2倍,容器的体积都为2L,所以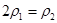 ,正确;D、三个容器的温度相同,则化学平衡常数相等,错误,答案选C;
,正确;D、三个容器的温度相同,则化学平衡常数相等,错误,答案选C;
(5)根据盖斯定律N2(g)+3H2(g)=2NH3(g)△H=-93.0kJ?mol-1,①
2 H2(g)+O2(g)="2" H2O(l) △H="-572" kJ?mol-1 ②
则2N2(g)+6H2O(l)="4" NH3(g)+3 O2(g)的△H=①×2-②×3="+1530" kJ?mol-,所以所求热化学方程式为
2N2(g)+6H2O(l)="4" NH3(g)+3 O2(g)△H=+1530kJ·mol-1
(6)氮气中的N元素化合价为0,氨气中的N元素的化合价为-3,所以氮气发生还原反应,则氮气是电解池的阴极;发生的电极反应式为N2+6H+++6e-==2 NH3
考点:考查化学平衡状态的判断,化学平衡常数的计算,盖斯定律的应用,电化学原理的应用,反应速率的计算

(7分)某同学模拟工业“折点加氯法”处理氨氮废水的原理,进行如下研究。
| 装置(气密性良好,试剂已添加) | 操作 | 现象 |
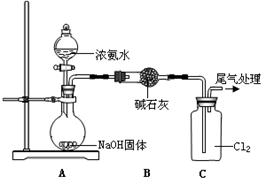 | 打开分液漏斗活塞,逐滴加入浓氨水 | ⅰ.C中气体颜色变浅 ⅱ.稍后,C中出现白烟并逐渐增多 |
(1)浓氨水分解可以制氨气,写出A中反应的化学方程式是 。从平衡移动 的角度分析NaOH固体在氨水分解中的作用 。
(2)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)= N2(g)+6HCl(g) ?H=—456 kJ·mol-1
已知:
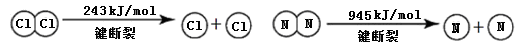
①NH3的电子式是 。
②断开1mol H-N键与断开1molH-Cl键所需能量相差约为 ,
(3)现象ⅱ中产生白烟的化学方程式是 。
(4)为避免生成白烟,该学生设计了下图装置以完成Cl2和NH3的反应。
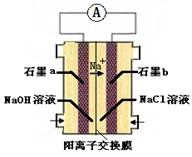
若该装置能实现设计目标,则①石墨b电极上发生的是 反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式: 。
(17分)CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物。工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气。
(1) 已知:CH4、H2和CO的燃烧热分别为890.3kJ/mol、285.8kJ/mol和283.0kJ/mol,且1mol液态水汽化时的能量变化为44.0kJ。写出甲烷与水蒸气在高温下反应制取合成气的热化学方程式 。
(2)在一定条件下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),测得CH4(g)和H2(g)的物质的量浓度随时间变化如下表所示:
  时间/min 时间/min物质 浓度 | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol·L—1 | 0.13 mol·L—1 | 0.1 mol·L—1 | 0.1 mol·L—1 | 0.09 mol·L—1 |
| H2 | 0 mol·L—1 | 0.2 mol·L—1 | 0.3 mol·L—1 | 0.3 mol·L—1 | 0.33 mol·L—1 |
②3min时改变的反应条件是____________________(只填一种条件的改变)
(3)已知温度、压强、投料比X〔n(CH4)/n(H2O)〕对该反应的影响如图所示。

①图1中的两条曲线所示投料比的关系X1____X2(填“=”“>”或“<”下同)
②图2中两条曲线所示的压强比的关系:p1_______p2
(4)以天然气(设杂质不参与反应)、KOH溶液为原料可设计成燃料电池
①放电时,正极的电极反应式_______________________________________
②设装置中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下的体积为8.96L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为 ____。
把煤作为燃料可通过下列两种途径:
途径I: C(s)+O2(g) = CO2(g)
途径II:先制水煤气: C(s) + H2O(g) =" CO(g)" + H2(g)
燃烧水煤气:2 CO(g) + O2(g) = 2CO2(g);
2H2(g)+O2(g) =2H2O(g)
已知:①C(s)+O2(g)=CO2(g);△H1=-393.5 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g);△H2=-241.8kJ·mol-1
③CO(g)+ 1/2O2 (g) =CO2(g);△H3=-283.0kJ·mol-1
请回答下列问题:
(1)CO(g) + H2O(g) = H2(g) + CO2(g) 是 (填“放热反应”或“吸热反应”)
(2)根据盖斯定律,煤和气态水生成水煤气的反应热△H= 。
(3)根据两种途径,下列说法错误的是( )
| A.途径II制水煤气时增加能耗,故途径II的做法不可取 |
| B.与途径I相比,途径II可以减少对环境的污染 |
| C.与途径I相比,途径II可以提高煤的燃烧效率 |
| D.将煤转化为水煤气后,便于通过管道进行运输 |
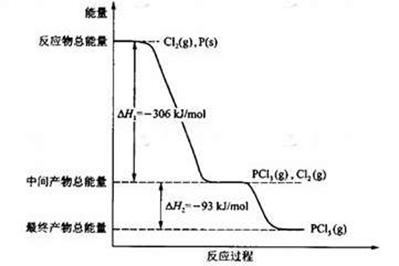
 1等于 ;若反应温度由T1升高到T2,平衡时PCl5的分解率为
1等于 ;若反应温度由T1升高到T2,平衡时PCl5的分解率为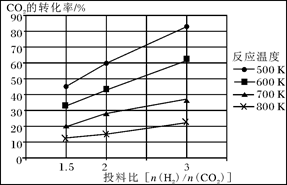
 CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)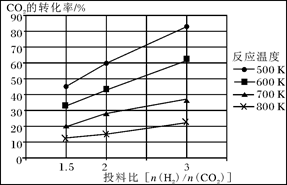
 H+(aq) +CH3COO-(aq) △H2="+1.3" kJ/mol
H+(aq) +CH3COO-(aq) △H2="+1.3" kJ/mol C6 H5- CH=CH2 (g) +H2(g) ΔH1
C6 H5- CH=CH2 (g) +H2(g) ΔH1