题目内容
20.下列关于乙醇和乙酸的说法正确的是( )| A. | 相互不能溶解 | B. | 都能使石蕊试液变红 | ||
| C. | 分子中都含有羧基 | D. | 在一定条件下能发生酯化反应 |
分析 A、绝大多数的有机物之间可以互溶;
B、-OH不能电离,显中性,而-COOH显酸性;
C、乙醇的结构简式为CH3CH2OH,乙酸为CH3COOH;
D、含有-OH或-COOH的有机物可以发生酯化反应.
解答 解:A、绝大多数的有机物之间可以互溶,乙醇和乙酸可以互溶,故A错误;
B、乙醇的结构简式为CH3CH2OH,-OH不能电离,显中性,不能使石蕊变红;乙酸为CH3COOH,而-COOH显酸性,能使石蕊变红,故B错误;
C、乙醇的结构简式为CH3CH2OH,结构中含羟基;乙酸为CH3COOH,结构中含羧基,故C错误;
D、含有-OH或-COOH的有机物可以发生酯化反应,而乙醇中含-OH,乙酸中含-COOH,故均能发生酯化反应,故D正确.
故选D.
点评 本题考查了乙醇和乙酸的结构、物理性质和化学性质,难度不大,掌握两者的结构从而理解性质是关键.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
11.根据下表部分短周期元素的原子半径及主要化合价信息回答以下问题:
(1)E与氢形成的化合物由两种分别是H2O、H2O2,其中心原子的杂化方式分别是sp3、sp3.
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
| 元素 | A | B | C | D | E | F | G | H |
| 原子半径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
15.下列物质属于多糖的是( )
| A. | 麦芽糖 | B. | 淀粉 | C. | 果糖 | D. | 核糖 |
5.在浓硫酸催化并加热的条件下,CH3COOH与CH3CH218OH发生酯化反应时,分子中含有18O的生成物是( )
| A. | 水 | B. | 乙酸乙酯 | C. | 硫酸 | D. | 氧气 |
10.元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
(1)请从上表中查出关于硼元素的一条信息:硼元素的相对原子量为10.81.
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的电子层数 相同.
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(选填“分子”、“原子”或“离子”).
(4)如图A、B、C是三种粒子的结构示意图.试回答下列问题:
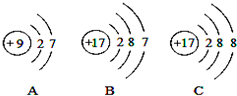
①A、B、C中属于同种元素的粒子是B和C;
②A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥIA | VIIA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的电子层数 相同.
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(选填“分子”、“原子”或“离子”).
(4)如图A、B、C是三种粒子的结构示意图.试回答下列问题:

①A、B、C中属于同种元素的粒子是B和C;
②A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质.
 .
. .
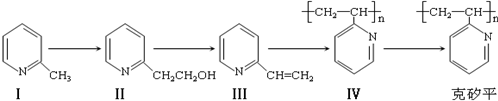
.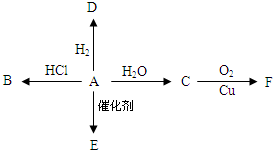 如图所示,已知有机物A的产量可以衡量一个国家的石油化工发展水平,A可以发生如图一系列的反应,按要求回答下列问题
如图所示,已知有机物A的产量可以衡量一个国家的石油化工发展水平,A可以发生如图一系列的反应,按要求回答下列问题