��Ŀ����
����Ŀ�����ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ����±�:����������ȷ����( )
Ԫ�ش��� | X | Y | Z | W |
ԭ�Ӱ뾶/pm | 160 | 143 | 70 | 66 |
��Ҫ���ϼ� | +2 | +3 | +5��+3��-3 | -2 |
A.X��WԪ�ص����Ӱ뾶 W<X
B.һ��������,W���ʿ�����ZԪ�ص��⻯�����ѧ��Ӧ
C.Y������������Ӧ��ˮ����������ϡ��ˮ
D.һ��������,Z������W�ij�������ֱ������ZW2
���𰸡�B
��������
X��Y��Z��W���Ƕ�����Ԫ�أ�W��-2�۴���VIA����WΪOԪ�أ�Z��+5��-3�ۣ�����VA�壬Z�İ뾶��O���Դ���ZΪNԪ�أ�X��Y��ԭ�Ӱ뾶��N��O�İ뾶��ܶ࣬��X��Y�ڵ������ڣ�X��+2�ۣ���XΪMg��Y��+3�ۣ���YΪAl��
A����������Ų���ͬ������£�ԭ������Խ�뾶ԽС�����O2-��Mg2+��A����
B��O2��NH3�ڴ����������¿��Է�����������![]() ��B��ȷ��
��B��ȷ��
C��Al(OH)3����ǿ�Ӧ�����ܸ����ˮ��Ӧ��C����
D��N2��O2�ڷŵ��������������NO������ֱ������NO2��D����
��ѡB��

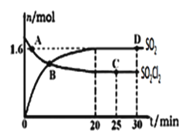
����Ŀ����300 mL���ܱ������У��������۲�����һ������CO���壬һ�������·�����Ӧ��Ni(s)��4CO(g)Ni(CO)4(g)����֪�÷�Ӧƽ�ⳣ�����¶ȵĹ�ϵ�����
�¶�/�� | 25 | 80 | 230 |
ƽ�ⳣ�� | 5��104 | 2 | 1.9��10��5 |
����˵������ȷ���ǣ� ��
A.���²���������Ӧ����Ni(CO)4(g)
B.��25 ��ʱ����ӦNi(CO)4(g)Ni(s)��4CO(g)��ƽ�ⳣ��Ϊ2��10��5
C.��80 ��ʱ,���ijʱ�̣�Ni(CO)4��COŨ�Ⱦ�Ϊ0.5 mol��L��1�����ʱv��>v��
D.��80 ��ﵽƽ��ʱ�����n(CO)��0.3 mol����Ni(CO)4��ƽ��Ũ��Ϊ2 mol��L��1
����Ŀ�����������(Na2S2O3)����Ҫ�Ļ���ԭ�ϣ������������Լ�������Ļ�ԭ����������ˮ�����ȡ������ֽ⡣Na2S2O3��5H2O����ɫ�����壬������ˮ����ϡ��Һ��BaCl2��Һ����������ɡ���ҵ�ϳ����ú����ˮ����Na2S2O3��5H2O��ij��ѧ��ȤС����ʵ����������ͼ��ʾװ��(����װ�ü����ּг�װ������ȥ)ģ�����������̲�̽���仯ѧ���ʡ�
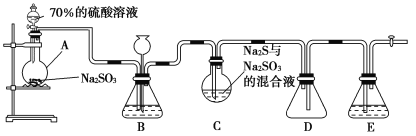
��ƿC�з������·�Ӧ��
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) ��
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) ��
S(s)+Na2SO3(aq)![]() Na2S2O3(aq) ��
Na2S2O3(aq) ��
��.�Ʊ�Na2S2O3��5H2O
(1)����ҩƷ֮ǰ����еIJ�����_________��װ��D��������______________��װ��B������֮һ�ǹ۲�SO2���������ʣ����е��Լ����ѡ��________(����ĸ)��
A.����ˮ�������������� B.����Na2SO3��Һ
C.����NaHSO3��Һ D.����NaHCO3��Һ
(2)Ϊ��֤��������ƵIJ�����ʵ���в�����SO2���ܹ�����ԭ����_________�����ƵõĴֲ�Ʒ����ͨ��________������һ���ᴿ�õ���Na2S2O3��5H2O��
��.�ⶨ��Ʒ����
ȷ��ȡw g��Ʒ������������ˮ�ܽ⣬�Ե�����ָʾ������0.10 mol��L��1I2�ı���Һ�ζ�����Ӧԭ��Ϊ2S2O32-+I2=S4O62-+2I-��
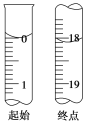
(3)�ζ����յ�ʱ������______________���ζ���ʼ���յ�ʱI2�ı���ҺҺ��λ����ͼ��ʾ��������I2�ı���Һ�����Ϊ________mL����Ʒ�Ĵ���Ϊ________(��Na2S2O3��5H2O����Է�������ΪM���г���M��w��ʾ�ı���ʽ)��
��.̽��Na2S2O3�IJ��ֻ�ѧ����
(4)��������裩��
����һ��Na2S2O3��Na2SO4�Ľṹ���ƣ���ѧ����ҲӦ�����ƣ���ˣ�����ʱNa2S2O3��Һ��pH=7��
���������S�Ļ��ϼ��Ʋ�Na2S2O3���н�ǿ�Ļ�ԭ�ԡ�
����֤���裩����������Na2S2O3��Һ����������ʵ�飬�뽫ʵ�鲹��������
ʵ����� | ʵ����� ������ | �������(������ ����ʽ��ʾ) | |
����һ | ________ | ��ҺpH=8 | ________ |
����� | ����ˮ�� �������� Na2S2O3 ��Һ | ��ˮ��ɫ | ________ |
ʵ����ۣ�________________________________________��
��.Na2S2O3��Ӧ��
(5)Na2S2O3����Ʒ��Ϊ�����������׳������մ�������ѧ�ϳ����ڵζ�ʵ�顣Ϊ�ⶨijK2Cr2O7��Һ��Ũ�ȣ��о�С���ͬѧȷ��ȡ10.00 mL K2Cr2O7��Һ����ƿ�У��������KI���������ϡH2SO4���μӼ���ָʾ������0.10 mol��L��1 Na2S2O3����Һ�ζ����յ㣬����3��ƽ��ʵ����ƽ������Na2S2O3��Һ�����Ϊ30.00 mL����c(K2Cr2O7)=________mol��L��1��(��֪��Cr2O72-+6I-+14H��=2Cr3++3I2+7H2O��2S2O32-+I2=S4O62-+2I-)
��.̽���뷴˼
(6)Ϊ��֤��Ʒ�к���Na2SO3��Na2SO4����С�����������ʵ�鷽�����뽫ʵ�鷽������������
ȡ������Ʒ���ϡ��Һ��___________________(�����Լ���BaCl2��Һ��ϡHNO3��ϡH2SO4��ϡ���ᡢ����ˮ��ѡ��)��