题目内容
8.T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的物质的量变化如图1所示,3分钟时达到平衡;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.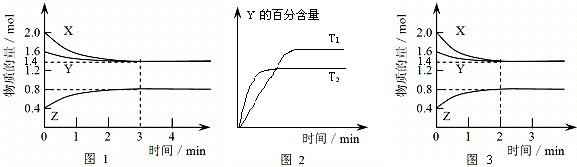
(1)容器中发生的反应可表示为3X(g)+Y(g)?2Z(g)
(2)反应进行的前3min内,用X表示的反应速率 v(X)=0.1mol/(L•min)
(3)保持其他条件不变,升高温度,该反应的化学平衡将向正反应方向移动(填“正反应”或“逆反应”)
(4)①若改变反应条件,使反应进程如图3所示,则改变的条件是催化剂
②一定条件下的密闭容器中,该反应达到平衡,要提高气体Y的转化率,可以采取的措施是ac(填字母代号).
a.高温高压 b.加入催化剂 c.减少Z的浓度 d.增加气体Y的浓度.
分析 (1)根据图示1可知:X、Y是反应物,Z是生成物,它们的物质的量的比等于3:2:1,由于最终各种物质都存在,所以该反应是可逆反应.故容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g);
(2)根据v=$\frac{△c}{△t}$计算出反应进行前3min内,用X表示的反应速率v(X);
(3)由图2可知,温度T2到达平衡需要的时间较短,故T2>T1,温度越高Y的含量降低,升高温度平衡向正反应方向移动;
(4)①图3与图1相比,平衡时各组分的物质的量不变,到达平衡时间缩短,说明改变条件,增大反应速率,平衡不移动,该反应正反应是气体体积减小的反应,增大压强平衡向正反应移动,不可能是增大压强,故改变条件是使用催化剂;
②a.高温高压,平衡向正向移动,气体Y的转化率增大;
b.加入催化剂,平衡不移动;
c.减少Z的浓度,平衡向正向移动,气体Y的转化率增大;
d.增加气体Y的浓度,虽然平衡向正向移动,但气体Y的转化率减小.
解答 解:(1)由图1知,X的物质的量减少量为:(2.0-1.4)mol=0.6mol,Y的物质的量减少量为:(1.6-1.4)mol=0.2mol,X、Y为反应物;Z的物质的量增加量为:(0.8-0.4)mol=0.4mol,Z为生成物,同一化学反应同一时间段内,反应物减少的物质的量和生成物增加的物质的量之比等于其计量数之比,所以X、Y、Z的计量数之比=0.6mol:0.2mol:0.4mol=3:1:2,所以反应可表示为:3X(g)+Y(g)?2Z(g),故答案为:3X(g)+Y(g)?2Z(g);
(2)反应进行前3min内,用X表示的反应速率为:v(X)=$\frac{\frac{2.0-1.4}{2}}{3}$=0.1mol/(L•min),故答案为:0.1mol;
(3)“先拐平数值大”,根据图2可知,T2>T1,升高温度后Y的含量减少,即平衡向正反应方向移动,故答案为:正反应;
(4)①由图3可知:各种物质在2min时就达到了平衡,但是物质的平衡浓度不变,所以平衡未发生移动,因为该反应是反应前后气体体积不等的可逆反应,则改变的条件是使用催化剂,故答案为:催化剂;
②a.高温高压,平衡向正向移动,气体Y的转化率增大,故正确;
b.加入催化剂,平衡不移动,故错误;
c.减少Z的浓度,平衡向正向移动,气体Y的转化率增大,故正确;
d.增加气体Y的浓度,虽然平衡向正向移动,但气体Y的转化率减小,故错误;
故选:ac.
点评 本题考查了化学平衡的图象及化学反应速率的计算、化学平衡的影响、平衡移动原理等,题目难度中等,根据图象正确分析曲线变化特点是解答本题的关键,结合平衡移动原理进行解答.

| A. | 一定有乙烯 | B. | 一定有甲烷 | ||
| C. | 可能有乙烷 | D. | 一定是甲烷和乙烯的混合物 |
| A. | C5H12 | B. | C17H36 | C. | C8H18 | D. | C6H14 |
| A. | 脂肪 | B. | 蛋白质 | C. | 葡萄糖 | D. | 纤维素 |
| A. | 实验室用大理石与醋酸反应制取二氧化碳:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯乙酸与足量的氢氧化钠溶液共热:CH2ClCOOH+OH-→CH2ClCOO-+H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO${\;}_{3}^{2-}$ | |
| D. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH- $\stackrel{水浴加热}{→}$CH3COO--+NH4++3NH3+2Ag↓+H2O |
Ⅰ火力发电燃烧煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如图所示:
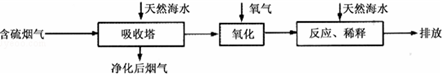
(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释主要原因CO32-+H2O?HCO3-+OH-或HCO3-+H2O?H2CO3+OH-.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是2H2SO3+O2═2H2SO4;氧化后的“海水”需要用大量的天然海水与之混后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸.
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=2c(SO32-)+c(HSO3-)(用含硫微粒浓度的代数式表示).
(4)相同物质的量的SO2与NH3溶于水发生反应的离子方程式为SO2+NH3•H2O=NH4++HSO3-,所得溶液中c(H+)-c(OH-)=BD (填字母编号).
A.c(SO32-)-c(H2SO3) B.c(SO32-)+c(NH3.H2O)-c(H2SO3)
C.c(HSO3-)+c(SO32-)-c(NH4+) D.c(HSO3-)+2c(SO32-)-c(NH4+)
Ⅱ重金属离子对河流及海洋造成严重污染.某化工厂废水(pH=2.0,ρ≈1g/mL)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.1mol/L.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶 电解质 | AgI | AgOH | Ag2S | pbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KI D.Ca(OH)2
(6)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=1.2×10-3mol•L-1.
( 7 )如果用食盐处理只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%(ρ≈1g•mL-1).若环境要求排放标准为c(Ag+)低于1.0×10-8mol/L,问该工厂处理后的废水中c(Ag+)=9×10-9 mol•L-1.(已知KSP(AgCl)=1.8×10-10)
 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.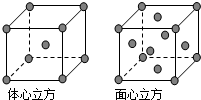 A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子.
A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子. ,分子中有2个σ键,2个π键.
,分子中有2个σ键,2个π键.