题目内容
19. (1)下列物质中,①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融NaOH ⑥稀硫酸 ⑦乙酸,属于强电解质且能导电的是⑤(填序号)
(1)下列物质中,①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融NaOH ⑥稀硫酸 ⑦乙酸,属于强电解质且能导电的是⑤(填序号)(2)已知:常温下0.1mol/L的某酸H2A的pH=4,则该酸为弱酸(填“强”或“弱”),该溶液中由水电离出的c(H+)=10-10mol/L.
(3)在常温下,将PH=3的硫酸与PH=11的氨水等体积混合,则所得混合溶液的PH=>7(填“>”、“=”或“<”).
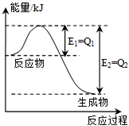
(4)如图是一定的温度和压强下N2(g)和H2(g)反应生成lmolNH3(g)过程中能量变化的示意图,请写出工业合成氨的热化学方程式:
(△H用含字母Q1、Q2的代数式表示)N2(g)+3H2(g)?2NH3(g)△H=2(Q1-Q2)KJ/mol;.
分析 (1)含有自由移动离子或电子的物质能导电,在熔融状态下或水溶液里能导电的化合物是电解质;
(2)在水溶液里只有部分电离的酸是弱酸,依据KW=c(H+)×c(OH-),pH=-lgc(H+)=4求解c(OH-),酸性溶液中水电离出的氢离子浓度等于溶液中氢氧根离子浓度;
(3)pH=3的硫酸溶液,与pH=11的氢氧化钠溶液中:c(H+)=c(OH-)=1×10-3mol/L,但一水合氨为弱碱,不完全电离,一水合氨浓度大,反应后剩余一水合氨;
(4)由图求出N2和H2反应生成1molNH3的反应热,再根据热化学反应方程式的书写要求解答.
解答 解:(1)①氯化钠溶液是混合物不是电解质;
②氯化铵固体是电解质,但是不含自由移动的离子或者电子,不导电;
③铜是单质,不是电解质;
④石墨是单质,不是电解质;
⑤熔融NaOH含有自由移动离子能够导电,在熔融状态下或水溶液里能导电的化合物,属于电解质;
⑥稀硫酸是混合物,不是电解质;
⑦乙酸不含不含自由移动的离子或者电子,不导电;
故答案为:⑤;
(2)pH=4溶液中,[H+]=10-4mol/L,0.1mol/L的某酸H2A的pH=4,说明H2A不能完全电离,所以是弱酸;
酸性溶液中水电离出的氢离子浓度等于溶液中氢氧根离子浓度,该溶液中由水电离出的c(H+)=c(OH-)=$\frac{Kw}{[{H}^{+}]}$$\frac{1{0}^{-14}}{10{\;}^{-4}}$=10-10mol/L,
故答案为:弱 10-10mol/L;
(3)pH=3的硫酸溶液,与pH=11的氢氧化钠溶液中:c(H+)=c(OH-)=1×10-3mol/L,但一水合氨为弱碱,不完全电离,一水合氨浓度大,反应后剩余一水合氨
溶液显碱性,所以pH>7;
故答案为:>;
(4)由图可知,N2和H2反应生成1molNH3放出的热量为(Q1-Q2)kJ,该反应的热化学反应方程式为N2(g)+3H2(g)?2NH3(g)△H=-2(Q1-Q2)kJ•mol-1,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=2 (Q1-Q2) KJ/mol.
点评 本题为综合题,考查了电解质的判断、弱电解质的电离及pH的有关计算,热化学方程式的书写,题目难度不大,掌握基础是解题关键.

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案反应②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2的平衡常数为K2,
反应③H2(g)+CO2(g)?CO(g)+H2O(g)△H=Q3,平衡常数为K3.
请结合表中在不同温度下K1、K2的值,回答下列问题:
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.20 | 1.50 |
(2)根据反应①与②推导出Q1、Q2、Q3的关系式:Q3=Q3=Q1-Q2.计算出在1173K时反应③的平衡常数K3的数值:K3=1.4.
(3)能判断反应③已达到化学平衡状态的依据是CD.
A.容器中压强不变 B.△H不变 C.v正(H2)=v逆(CO) D.CO的质量分数不变.
| A. | 水玻璃保存在带磨口玻璃塞的试剂瓶中 | |
| B. | 少量金属钠可保存在煤油中,大量的金属钠可保存在液体石蜡中 | |
| C. | 氢氟酸保存在磨口试剂瓶中 | |
| D. | 液溴密封盛放在无色试剂瓶中,并在液面上放一层水 |
| A. | c(H+)=c(Cl-)+c(OH-) | |
| B. | 由水电离出的c(H+)=1.0×10ˉ 2 mol•Lˉ1 | |
| C. | 与等体积PH=12的氨水混合后所得溶液显中性 | |
| D. | 与等体积0.01 mol•Lˉ1CH3COONa溶液混合后所得溶液中:c(Cl-)=c(CH3COO-) |
| A. | 盐酸与碳酸钠,盐酸与碳酸钙 | |
| B. | 氯化钡与硫酸钠,氢氧化钡与硫酸镁 | |
| C. | 氢氧化钠与盐酸,氢氧化钠与醋酸 | |
| D. | 硝酸钙与碳酸钠,氯化钙与碳酸钾 |
| A. | 葡萄糖 | B. | 蛋白质 | C. | 乙醇 | D. | 芝麻油 |