题目内容
【题目】现有下列几种有机物:A.CH4 B.(CH3)2C=CH﹣CH3 C.C2H2 D.C6H14 E.CH2=CH﹣CH=CH2 F.环戊烷
(1)上述有机物中互为同系物的是______(填序号,下同),互为同分异构体的是________;
(2)用系统命名法对B进行命名________________;
(3)实验室制取C的反应的化学方程式为_________________;
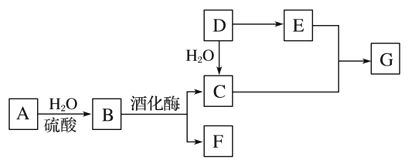
(4)下图表示的是一种叫做双烯合成的有机反应,请写出 B 与 E发生双烯合成所得产物的结构简式____。
![]()
【答案】AD BF 2﹣甲基﹣2﹣丁烯 CaC2+2H2O→Ca(OH)2+C2H2↑ 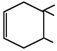
【解析】
A.CH4属于烷烃;B.(CH3)2C=CH﹣CH3属于单烯烃,分子式为C5H10;C.C2H2属于炔烃;D.C6H14属于烷烃;E.CH2=CH﹣CH=CH2属于二烯烃,分子式为C4H6;F.环戊烷属于环烷烃,分子式为C5H10;
(1)同系物,是指结构相似、分子组成相差若干个“CH2”原子团的有机化合物,上述有机物中CH4和C6H14均属于烷烃,互为同系物的是AD;B.(CH3)2C=CH﹣CH3 和 F.环戊烷的分子式均为C5H10,分子式相同,结构不同,故互为同分异构体的是BF;故答案为:AD;BF;
(2)(CH3)2C=CH﹣CH3 含碳碳双键的主链是4个碳,双键在2号碳与3号碳之间,2号位有甲基,B的系统名称为2﹣甲基﹣2﹣丁烯;故答案为:2﹣甲基﹣2﹣丁烯;
(3)实验室用电石和饱和食盐水制取C2H2,反应的化学方程式为CaC2+2H2O→Ca(OH)2+C2H2↑;故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(4) B 与 E发生双烯合成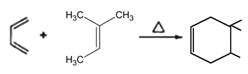 ,所得产物的结构简式
,所得产物的结构简式 。故答案为:
。故答案为: 。
。

【题目】汽车尾气中含有CO、NO等有害气体。
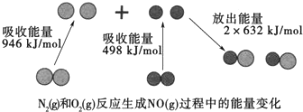
(1)汽车尾气中NO生成过程的能量变化如图示。1molN2和1molO2完全反应生成NO会____(填“吸收”或“放出”)____kJ能量。
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:(提示:O2-可在此固体电解质中自由移动)
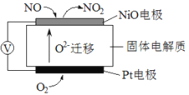
①NiO电极上发生的是___________反应(填“氧化”或“还原”)。
②外电路中,电子是从_________电极流出(填“NiO”或“Pt”).
③Pt电极上的电极反应式为________________________。
(3)一种新型催化剂用于NO和CO的反应:2NO+2CO![]() 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
实验编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.2×10﹣3 | 5.80×10﹣3 | 82 |
Ⅱ | 280 | 1.2×10﹣3 | b | 124 |
Ⅲ | 350 | a | 5.80×10﹣3 | 82 |
①请将表中数据补充完整:a ___________。
②能验证温度对化学反应速率规律的是实验____________(填实验序号)。
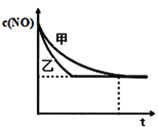
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线_______(填“甲”或“乙”)。
(4)在容积固定的绝热容器中发生反应2NO+2CO![]() 2CO2+N2,不能说明已达到平衡状态的是________(不定项选择);
2CO2+N2,不能说明已达到平衡状态的是________(不定项选择);
A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2υ逆(NO)=υ正(N2) D.容器内混合气体密度保持不变
【题目】已知:pAg=-lgc(Ag+),pX=-lg c(Xn-)。298K时,几种物质的Ksp如下表:
化学式 | AgCl | AgSCN | Ag2CrO4 |
颜色 | 白 | 浅黄 | 红 |
Ksp | 1.8×1010 | 1.0×1012 | 2.0×1012 |
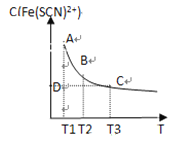
AgCl、AgSCN、Ag2CrO4的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
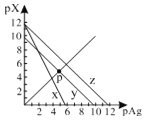
A.图中x代表AgCl曲线,z代表AgSCN曲线
B.298K时,在Cl-和CrO42-的物质的量浓度均为0.1mol/L的溶液中,滴入少量0.1mol/L的AgNO3溶液,首先产生的是红色沉淀
C.298K时若增大p点的阴离子浓度,则y上的点沿曲线向上移动
D.298K时Ag2CrO4(s)+2SCN-(aq) ![]() 2AgSCN(s)+CrO42- (aq)的平衡常数K=2.0×1012
2AgSCN(s)+CrO42- (aq)的平衡常数K=2.0×1012