��Ŀ����
11��������������Ԫ��֮һ����ȱ���Ỽ�����Ӳ�������ɶ�ͯ�������£�Ϊ��������ȱ���������ҹ涨��ʳ���мӵ�����ǿ���Ӫ������1������ĵ�ָ����b��a���ⵥ�ʣ�b��Ԫ�أ���
��2��С��ͨ���������ϵ�֪���ⵥ�������۱�����KI����ǿ��ԭ�ԣ��ڿ������ױ�������I2����KIO3�����������¾���ǿ�������ܣ���KI�������·�Ӧ��IO3-+5I-+6H+�T3I2+3H2O������Ϊʳ�μӵ⣬�Ǽ�KI�û��Ǽ�KIO3�ã�KIO3��������KIO3���ʽ��ȶ���
��3��С����ͨ��ʵ�����������ijƷ�Ƶ�ʳ�����Ƿ�IO3-������������ʦҪ��һЩKI�����ӳ���ȡ��һƿʳ������ʳ�Σ�����Ϊ��������ʲô���ʣ����ۣ�С��������Ҫ��Щ�������Թܡ�ҩ�ס���ͷ�ιܣ�
���� ��1��ʳ�μӵⲻ�����ӵⵥ�ʣ�
��2��KI�ڿ������ױ�������I2��KIO3���ʽ��ȶ���
��3���ⵥ�������۱���ɫ�������Թ��з�Ӧ��
��� �⣺��1��ʳ�μӵ����ӵ���أ���ָ��Ԫ�أ��ʴ�Ϊ��b��
��2��KI�ڿ������ױ�������I2��KIO3���ʽ��ȶ�����KIO3�ã��ʴ�Ϊ��KIO3��KIO3���ʽ��ȶ���
��3���ⵥ�������۱���ɫ��ȱ�ٵ��ۣ�����ҩ��ȡ�ù��壬��ͷ�ι�ȡ��Һ�壬���Թ��з�Ӧ���ʴ�Ϊ�����ۣ��Թܡ�ҩ�ס���ͷ�ιܣ�
���� ���⿼����Ԫ���Լ���ѧʵ��ȣ�Ϊ��Ƶ���㣬���ػ�ѧ����������Լ������Ŀ��飬����������ѧ�������õĿ�ѧ�������ѶȲ���

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
1�����з�Ӧ�У��������ȷ�Ӧ���ǣ�������
| A�� | ���������������Ȼ�茶��巴Ӧ | B�� | ������������ȼ�� | ||
| C�� | ����������Һ�����ᷴӦ | D�� | ����ˮ��Ӧ |
2�����и���Һ�У��ֱ����Na2O2��ȷų��������й����������ǣ�������
| A�� | FeCl3ϡ��Һ | B�� | NaClϡ��Һ | C�� | ����Ca��OH��2��Һ | D�� | ����NaHCO3��Һ |
19�����е��뷽��ʽ����ȷ���ǣ�������
| A�� | Na2CO3$\frac{\underline{\;ͨ��\;}}{\;}$2Na++CO32- | B�� | MgSO4�TMg2++SO42- | ||
| C�� | NaHCO3�TNa++H++CO32- | D�� | NaHSO3$\frac{\underline{\;����\;}}{\;}$Na++H++SO42- |
16�������й���������Ӧ�ĵ�λ���������ǣ�������
| A�� | Ħ������g•mol-1 | |
| B�� | ����Ħ�����L•mol-1 | |
| C�� | ��ԭ�ӵ�Ħ�����������������ԭ������ | |
| D�� | һ����ԭ�ӵ�����Լ����$\frac{23}{6.02��1{0}^{23}}$g |
7����ҵ�ϳ��Ը������������ķ�ҺΪԭ������������������Ҫ�������£�
��Һ$��_{��}^{�ᴿ���ᾧ}$FeSO4•7H2O$\stackrel{��}{��}$FeSO4��Һ$��_{��}^{NH_{4}HCO_{3}��Һ}$FeCO3$\stackrel{��}{��}$Fe2O3
��1����֪����������������ڲ�ͬ�¶��µ��ܽ�Ⱥ����������������±���ʾ��
��������������Һ�нᾧ��FeSO4•7H2O�����Ƶ��¶ȣ�t��Ϊt��56.7�森
��2����������һ�������ᣬ����ҪĿ��������FeSO4��ˮ�⣮
��3������FeCO3��Һ�����ӷ���ʽΪFe2++2HCO3-�TFeCO3��+CO2��+H2O��FeCO3��Һ¶���ڿ����л���ֺ��ɫ�Ĺ��壬�ñ仯�Ļ�ѧ����ʽΪ4FeCO3+6H2O+O2�T4Fe��OH��3+4CO2��
��4����֪FeSO4•7H2O��Һ�����ڼ��������·������·�Ӧ��FeSO4•7H2O$\frac{\underline{\;����\;}}{\;}$Fe2O3+SO2��+SO3��+14H2O����������ͼװ�ÿɼ���÷�Ӧ��������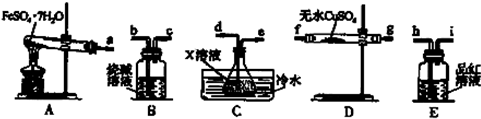
����д���пհף�
������������˳��Ϊa��f����g����g����f����d��e��h��i��b��
��װ��C�е�XΪ�Ȼ�����Һ��
��Һ$��_{��}^{�ᴿ���ᾧ}$FeSO4•7H2O$\stackrel{��}{��}$FeSO4��Һ$��_{��}^{NH_{4}HCO_{3}��Һ}$FeCO3$\stackrel{��}{��}$Fe2O3
��1����֪����������������ڲ�ͬ�¶��µ��ܽ�Ⱥ����������������±���ʾ��
| �¶�/�� | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | ||
| �ܽ��/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 | ||
| �������� | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
��2����������һ�������ᣬ����ҪĿ��������FeSO4��ˮ�⣮
��3������FeCO3��Һ�����ӷ���ʽΪFe2++2HCO3-�TFeCO3��+CO2��+H2O��FeCO3��Һ¶���ڿ����л���ֺ��ɫ�Ĺ��壬�ñ仯�Ļ�ѧ����ʽΪ4FeCO3+6H2O+O2�T4Fe��OH��3+4CO2��
��4����֪FeSO4•7H2O��Һ�����ڼ��������·������·�Ӧ��FeSO4•7H2O$\frac{\underline{\;����\;}}{\;}$Fe2O3+SO2��+SO3��+14H2O����������ͼװ�ÿɼ���÷�Ӧ��������

����д���пհף�
������������˳��Ϊa��f����g����g����f����d��e��h��i��b��
��װ��C�е�XΪ�Ȼ�����Һ��