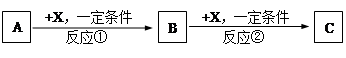题目内容
A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)。
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为 ;
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则
①C的化学式为 ;
②反应B+A→C的离子方程式为 ;
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D的化学式为 ;
②若图c符合事实,则其pH变化的原因是 (用离子方程式表示);
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式: 。
(1)3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(2)①Al(OH)3②Al3++3AlO2-+6H2O=4Al(OH)3↓
(3)①CO2②2HSO3-+O2=2H++2SO42-
(4)C(s)+1/2O2(g)="CO(g)" ⊿H=-110.6kJ/mol
解析试题分析:(1)A为金属单质,随D酸的稀溶液的量的不同而产物不同,故A是变价金属,故是Fe,D酸具有氧化性,稀溶液具有氧化性的酸是HNO3,故C+D→B反应为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;(2)A、B为盐,A随强碱D溶液的量的不同而产物不同,A的水溶液显酸性,则是Al3+,C为Al(OH)3,B+A→C为Al3++3AlO2-+6H2O=4Al(OH)3↓;(3)A为强碱,D为气态氧化物,D为二元酸酸酐,可以是CO2或SO2,b图是pH不变,为CO2;pH减小的是SO2,因为亚硫酸在空气中易氧化为硫酸使pH减小,即2HSO3-+O2=2H++2SO42-;(4)A为非金属单质,空气主要成分D易反应是O2,能量关系看出反应计量:A+ O2→C,C+
O2→C,C+ O2→B,A元素有+2、+4价,故A是碳,A+D→C的热化学方程式是C(s)+
O2→B,A元素有+2、+4价,故A是碳,A+D→C的热化学方程式是C(s)+ O2(g)="CO(g)" ⊿H=-110.6kJ/mol。
O2(g)="CO(g)" ⊿H=-110.6kJ/mol。
考点:元素单质及其化合物之间的转化。

下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| B | 将少量某无色气体通入澄清石灰水 | 出现白色沉淀 | 该气体一定是CO2 |
| C | 分别用测定常温下0.1 mol·L--1 Na2SiO3和Na2CO3的PH | PH:Na2SiO3﹥Na2CO3 | 非金属性Si﹥C |
| D | 向浓度均为0.1 mol·L-1NaCl和NaI混合溶液中, 滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
下列叙述正确的是
| A.硅是一种重要的非金属单质,可用于制造太阳能电池 |
| B.硫在足量的空气中燃烧生成SO3 |
| C.钠在空气中燃烧生成氧化钠 |
| D.与同浓度稀盐酸反应的速率:Na2CO3>NaHCO3 |
下列有关物质的性质和该性质的应用均正确的是
| A.H2O2是一种绿色氧化剂,可与酸性高锰酸钾作用产生 |
| B.SiO2晶体硅具有半导体性质,可用于生产光导纤维 |
| C.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸 |
| D.铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料 |
X、Y、Z、W是元素周期表前四周期的常见元素,其相关信息如下表:
| X | X的一种核素的质子数为56,中子数为30 |
| Y | 海水中元素含量最高的金属元素 |
| Z | 常温常压下,Z单质是淡黄色固体,常在火山口附近沉积 |
| W | 价电子的排布式为3s23p3 |
(1)Z元素在元素周期表中的位置为 ,Z的电负性比W的 (填“大”或“小”)。
(2)X元索的基态原子电子排布式是 _ ,其有___种运动状态不同的电子。该元素的白色氧氧化物在空气中会迅速变成灰绿色。最后变成红褐色、其反应的化学方程式为 。
(3)Y的单质在工业上用途广泛,工业上以YW制取Y单质的化学方程式为 。
(4)设计实验验证Z和W的非金属性的强弱: 。