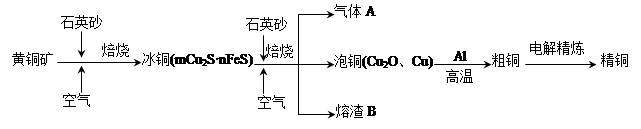��Ŀ����
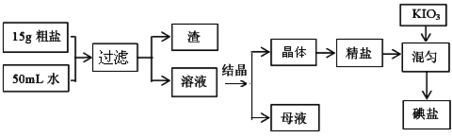
��ͼ��ij�о���ѧϰС����ƵĶ�һ�ַϾɺϽ���ɷ֣�����Cu��Fe��Si ���ֳɷ֣����з��롢���������õĹ�ҵ���̣�ͨ�������̽����ɷ�ת��Ϊ���õĵ��ʼ������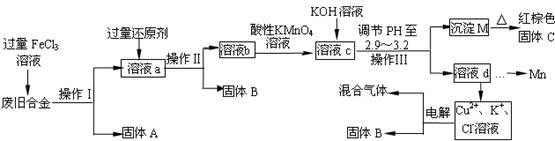
��֪��298Kʱ��Ksp[Cu(OH)2]=2��2��10-20��Ksp[Fe(OH)3]=4��0��10-38��Ksp[Mn(OH)2]=1��9��10-13��
�����������̻ش��й����⣺
��1��������ָ���� ��
��2���������FeCl3��Һ�����п����漰�Ļ�ѧ����ʽ�� ��
��3�������Ļ�ԭ��Ӧ�� ����Һb�������Ľ����������� ��
��4��������Һb�м�������KMnO4��Һ������Ӧ�����ӷ���ʽΪ ��
������Xmol/LKMnO4��Һ������Һb����ǡ�÷�Ӧʱ����KMnO4��ҺYmL����������ú���ɫ����C������Ϊ g���ú�X��Y�Ĵ���ʽ��ʾ����
��5��������,����Һc�������Ľ���������Ũ����ȣ�����Һc����μ���KOH��Һ�������ֽ��������ӳ������Ⱥ�˳��Ϊ�� �� �� ��(�����������)
��6�����һ��������ö��Ե缫���һ��ʱ�����������B������ΪZg��ͬʱ������������ռ��������������ȣ��������������ɵ����һ���������Ϊ L���ú�Z�Ĵ���ʽ��ʾ����
��1�����ˣ�1�֣�
��2��2FeCl3 +Fe = 3FeCl2��2�֣�, 2FeCl3 + Cu= 2FeCl2 +CuCl2��2�֣�
��3��Cu�ۣ�1�֣� Cu2+,Fe2+ ��1�֣�
��4����MnO4- + 5Fe2+ + 8H+= Mn2++ 5Fe3++4H2O��2�֣� ��0��4XY��2�֣�
��5��Fe3+��Cu2+��Mn2+��1�֣�
��6��22��4Z/64 ��2�֣�
���������������1�������̿�֪������ָ���ǹ��ˣ�
��2���������FeCl3��Һʱ�ķ�ӦΪ��2FeCl3 +Fe = 3FeCl2, 2FeCl3 + Cu= 2FeCl2 +CuCl2��
��3�����������ͭ�ۿɽ�������FeCl3 ��ԭΪFe2+������Һb�еĽ���������ΪCu2+,Fe2+ ��
��4�����з�Ӧ�����ӷ���ʽΪMnO4- + 5Fe2+ + 8H+= Mn2++ 5Fe3++4H2O��Ϸ���ʽ�ɼ���ú���ɫ��Fe2O3Ϊ0��4XY g��
��5����Ϊ298Kʱ��Ksp[Cu(OH)2]=2��2��10-20��Ksp[Fe(OH)3]=4��0��10-38��Ksp[Mn(OH)2]=1��9��10-13������Һc�н���������Ũ����ȣ���������������ӳ������Ⱥ�˳��ΪFe3+��Cu2+��Mn2+��
��6���Զ��Ե缫�����Һ������ӦʽΪCu2++2e-=Cu H++2e-=H2����������ӦʽΪ2Cl--2e-=Cl2�� , 4OH--4e-=O2��+2H2O,�������������������������ʵ����ֱ�Ϊa��x��y��ת�Ƶ��ӷֱ�Ϊ2a��2x��4y��
��Ϊ�����ռ���������ȣ���a=x+y �٣��ɵ�ʧ�����غ��2a+(Z/64)��2=2x+4y ��;��-�١�2��y=Z/64,������ñ�������Ϊ22��4Z/64��
���㣺Ԫ�ػ�����֪ʶ�����ӷ���ʽ�����ԭ����

�����й����ʵ����ʻ�Ӧ�ò���ȷ���ǣ� ��
| A����ʹ�ô�����Һ��ϴ����ʱ�����ȿ�����ǿ��ȥ������ |
| B��Һ������ʱҪ���մ������ȣ���˰���������� |
| C����AlCl3��Һ�м����������������Һ���Ʊ��������� |
| D����¯ˮ���к��е�CaSO4��������Na2CO3��Һ���������ô����ȥ |
������������װ����֤��Ũ����������п��Ӧʱ�ɵõ�SO2��H2�������壬�����Լ���ѡ��
(1)������ķ����У�����ʵ������ʵ��Ŀ�ĵ�װ��ʾ��ͼ(����ѡ������ͼ���г�װ�á����ӽ��ܡ���Ƥ����β������װ�ò��ػ�����Ҳ���ر��װ�����Լ�����Ҫ���ȵ������·��á����)��������������ÿ�������·������ĸA��B��C����������ѡ�õ�����(��������)���ױ�ʾ���£�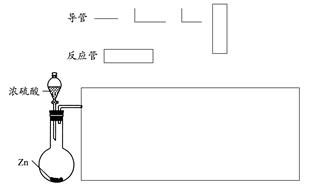
(2)���ݷ����е�װ��ͼ����д�±���
| �������� | �������������� | ���� |
| | | |
| ���һ��װ��(��ͼʱ�������) | Ũ���� | ��ֹ������ˮ��������E�и���ʵ�� |