题目内容
19.下列溶液中溶质的物质的量浓度为1mol/L的是( )| A. | 含K+为2mol的K2SO4溶液 | |
| B. | 将58.5gNaCl溶解于1L水中 | |
| C. | 将0.5mol/L的NaNO3溶液100mL加热蒸发掉50克水的溶液 | |
| D. | 将80gSO3溶于水并配成1L溶液 |
分析 A、物质的量浓度=$\frac{溶质的物质的量}{溶液体积}$;
B、58.5g氯化钠的物质的量为1mol,溶于1L水中,溶液的体积大于1L;
C、100mL溶液蒸发掉50g水,剩余溶液体积未知,不能计算物质的量浓度;
D、80g三氧化硫的物质的量为1mol,配成1L溶液,溶液的体积为1L,据此解答即可.
解答 解:A、由于为告诉溶液的体积,故不能计算硫酸钾溶液的物质的量浓度,故A错误;
B、58.5gNaCl溶解于1L水中,溶液的体积大于1L,故浓度小于1mol/L,故B错误;
C、蒸发掉50g水后,剩余溶液未告诉密度,无法计算溶液的体积,故C错误;
D、80gSO3的物质的量=$\frac{80g}{80g/mol}$=1mol,溶于水配制成1L溶液,物质的量浓度=$\frac{1mol}{1L}$=1mol/L,故D正确,故选D.
点评 本题考查学生对物质的量浓度的理解,比较基础,容易出错的是B选项,注意物质的量浓度计算当中的体积为溶液的体积.

练习册系列答案
相关题目
9.下列关于有机物的说法中,错误的是( )
| A. | 乙烯常温下是气体,聚乙烯常温下是固体 | |
| B. | 苯可做有机溶剂 | |
| C. | 乙醇和乙烯都能发生加成反应 | |
| D. | 油脂可用来制造肥皂 |
10.设NA为阿佛加德罗常数的值,下列叙述正确的是( )
| A. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3mol I2转移的电子数为5NA个 | |
| B. | 电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g | |
| C. | 在反应3Cl2+8NH3═6NH4Cl+N2中,有1.2NA个电子发生转移,则被氧化的氨气的质量是27.2 g | |
| D. | 等物质的量的CH4和CO所含分子数均为NA |
7.25℃的四种溶液:
①pH=2的CH3COOH溶液②pH=2的HCl溶液③pH=12的氨水④pH=12的NaOH溶液,
有关上述溶液的说法,正确的是( )
①pH=2的CH3COOH溶液②pH=2的HCl溶液③pH=12的氨水④pH=12的NaOH溶液,
有关上述溶液的说法,正确的是( )
| A. | ①、④溶液中水电离的c( H+):①>④ | |
| B. | 将②、③溶液混合后pH=7,则消耗溶液的体积:②<③ | |
| C. | 将①、④溶液混合后pH=8,则c(Na+)-c(CH3COO-)=9.9×10-7mol•L-1 | |
| D. | 分别向等体积的上述溶液中加入100 mL,水,溶液的pH:③>④>①>② |
14.将KCl和CrCl3两种固体混合物共熔发生化合反应制得化合物X.将1.892gX中Cr元素全部氧化成Cr2O72-,Cr2O72-可与过量的KI发生氧化还原反应氧化出2.667g I2,反应的离子方程式是:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,如果取溶有1.892g X的溶液,加入过量的AgNO3,可得4.52gAgCl沉淀,则表示X组成的化学式为( )
| A. | K3Cr2Cl7 | B. | K3Cr2Cl5 | C. | K3Cr2Cl9 | D. | K2CrCl4 |
11.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 在反应4FeS2+11O2=2Fe2O3+8SO2中,每生成1molSO2转移电子数为5.5NA | |
| B. | 标准状况下,11.2LO2参加反应转移的电子数一定为2NA | |
| C. | t℃时,MgCO3的Ksp=4×10-6,则饱和溶液中含Mg2+数目为2×10-3NA | |
| D. | 50g46%的乙醇水溶液中,含氢原子总数目为3NA |
8.新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化.某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式如下:下列说法正确的是( )
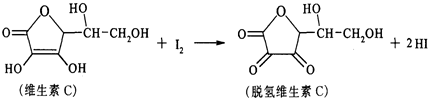

| A. | 上述反应为 取代反应 | |
| B. | 维生素C在酸性条件下水解只得到1种产物 | |
| C. | 滴定时可用淀粉溶液作指示剂 | |
| D. | 维生素C的分子式为C6H10O6 |
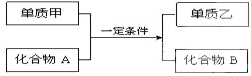
 已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化物A起反应.据此,请填空:
已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化物A起反应.据此,请填空: