题目内容
【题目】![]() 是高炉炼铁的重要反应。下列关于该反应的说法正确的是
是高炉炼铁的重要反应。下列关于该反应的说法正确的是![]()
A.CO是氧化剂B.CO得到电子
C.![]() 被还原D.
被还原D.![]() 发生氧化反应
发生氧化反应
【答案】C
【解析】
A.由Fe2O3+3CO ![]() 2Fe+3CO2反应可知,C元素的化合价由+2价变为+4价,化合价升高,CO发生氧化反应,CO作还原剂,故A错误;
2Fe+3CO2反应可知,C元素的化合价由+2价变为+4价,化合价升高,CO发生氧化反应,CO作还原剂,故A错误;
B.由Fe2O3+3CO ![]() 2Fe+3CO2反应可知,C元素的化合价由+2价变为+4价,化合价升高,失去电子,故B错误;
2Fe+3CO2反应可知,C元素的化合价由+2价变为+4价,化合价升高,失去电子,故B错误;
C.由Fe2O3+3CO ![]() 2Fe+3CO2反应可知,Fe元素的化合价由+3价变为0价,化合价降低,得到电子,Fe2O3被还原,故C正确;
2Fe+3CO2反应可知,Fe元素的化合价由+3价变为0价,化合价降低,得到电子,Fe2O3被还原,故C正确;
D.由Fe2O3+3CO ![]() 2Fe+3CO2反应可知,Fe元素的化合价由+3价变为0价,化合价降低,Fe2O3发生还原反应,故D错误;
2Fe+3CO2反应可知,Fe元素的化合价由+3价变为0价,化合价降低,Fe2O3发生还原反应,故D错误;
答案为C。

 名校课堂系列答案
名校课堂系列答案【题目】碳及其化合物在化工生产中有着广泛的应用。
I.为解决大气中CO2的含量增大的问题,某科学家提出如下构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,在合成塔中经化学反应使废气中的CO2转变为燃料甲醇。部分技术流程如下:
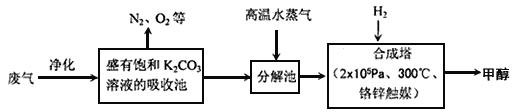
⑴合成塔中反应的化学方程式为_________;△H<0。该反应为可逆反应,从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了_____。
(2)从合成塔分离出甲醇的原理与下列_______操作的原理比较相符(填字母)
A.过滤 B.分液 C.蒸馏 D.结晶
(3)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。写出CO2(g)与H2(g)反应生CH4(g)与液态水的热化学方程式_____。
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=-890.3kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ/mol
II.某兴趣小组模拟工业合成甲醇的反应:CO(g)+2H2(g)![]() CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:
CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:
时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/Mpa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(1)从反应开始到20min时,以CO表示反应速率为________。
(2)下列描述能说明反应达到平衡的是_______
A.装置内气体颜色不再改变 B.容器内气体的平均摩尔质量保持不变
C.容器内气体的压强保持不变 D.容器内气体密度保持不变
(3)该温度下平衡常数K=_______,若达到平衡后加入少量CH3OH(g),此时平衡常数K值将_________ (填“增大”、“减小”或“不变”)
(4)该反应达到平衡后,再向容器中充入1mol CO和2mol H2,此时CO的转化率将_____(填“增大”、“减小”或“不变”)
Ⅲ. 人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:
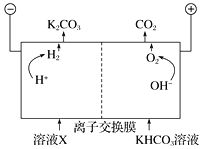
①在阳极区发生的反应包括_________和H++HCO![]() ===H2O+CO2↑。
===H2O+CO2↑。
②简述CO32-在阴极区再生的原理:______。