题目内容
【题目】硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4。回答下列问题:
(1)写出基态Zn原子的价电子排布式__,基态S原子核外未成对电子数为__。
(2)ZnSO4中三种元素的电负性由大到小的顺序为__,SO42-的立体构型为__,其中S的杂化轨道类型为__。
(3)硫酸锌溶于氨水可生成[Zn(NH3)4]SO4溶液,[Zn(NH3)4]SO4溶液中不存在的微粒间作用力有__。
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
(4)根据下列锌卤化物的熔点和溶解性,分析ZnCl2、ZnBr2、ZnI2熔点依次增大的原因__。
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
熔点/℃ | 872 | 275 | 394 | 446 |
在乙醇、乙醚中溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
(5)钾晶体晶胞结构如图所示,距离最近的两个钾原子距离为acm,阿伏加德罗常数为NA。
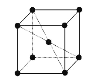
①钾原子核外运动状态不同的电子数是___。
②钾晶体的密度是___。
【答案】3d104s2 2 O、S、Zn 正四面体形 sp3 a ZnCl2、ZnBr2、ZnI2都是分子晶体,组成与结构相似,随着相对分子质量的增大,范德华力增强,熔沸点升高 19 ![]()
【解析】
(1)Zn位于周期表中第四周期,第IIB族,结合Zn的核外电子排布式解答,S是氧族元素,价电子排布式为3s23p4,p轨道上有未成对电子;
(2)ZnSO4中三种元素为Zn,S,O,非金属元素的电负性普遍大于金属元素,根据VSEPR理论和杂化轨道理论判断![]() 的立体构型,等电子原理是原子数相同的条件下,原子的价电子数相同,据此解答;
的立体构型,等电子原理是原子数相同的条件下,原子的价电子数相同,据此解答;
(3)[Zn(NH3)4]SO4为配合物,其溶于水后完全电离出[Zn(NH3)4]2+和![]() ,根据离子中存在的化学键判断;
,根据离子中存在的化学键判断;
(4)乙醇、乙醚都是有机溶剂,根据相似相溶原理,溶解的应是结构相似的物质,也就是溶质分子的分子间力与溶剂分子之间的分子间力越相似,越易互溶;分子晶体组成相似,随着相对分子质量增大,分子间作用力增强,熔沸点上升;
(5)①钾原子核电荷数为19,原子核外有19个电子;
②晶胞中顶点钾原子和中心钾原子距离最近,且两个钾原子距离为acm,则晶胞的边长为![]() cm,晶胞的体积为
cm,晶胞的体积为![]() cm3,晶胞中K原子数目为8×
cm3,晶胞中K原子数目为8×![]() +1=2,晶胞的质量为
+1=2,晶胞的质量为![]() g,据此计算钾晶体的密度。
g,据此计算钾晶体的密度。
(1)基态Zn原子在元素周期表中所处的位置是第四周期,第IIB族,基态Zn的价电子排布式为3d104s2;S元素为氧族元素,价电子排布式为3s23p4,3p轨道排4个电子,其中只有一对是成对的,剩余2个为单电子,因此未成对电子数为2;
(2)ZnSO4中三种元素为Zn,S,O,非金属元素的电负性普遍大于金属元素,同主族元素从上到下,电负性值逐渐减少,因此电负性顺序为O>S>Zn;对于![]() ,根据VSEPR理论,
,根据VSEPR理论,![]() 中,与中心S原子的成键原子数为BP=4,孤电子对数为
中,与中心S原子的成键原子数为BP=4,孤电子对数为![]() =0,则价电子对数为4+0=4,根据杂化轨道理论可知S原子为sp3杂化,则
=0,则价电子对数为4+0=4,根据杂化轨道理论可知S原子为sp3杂化,则![]() 的立体构型为正四面体形;
的立体构型为正四面体形;
(3)[Zn(NH3)4]SO4为配合物,其溶于水后完全电离出[Zn(NH3)4]2+和![]() ,则溶液中不存在离子键,H2O、
,则溶液中不存在离子键,H2O、![]() 和NH3内存在的作用力为共价键,[Zn(NH3)4]2+内存在配位键,水分子间存在范德华力和氢键,
和NH3内存在的作用力为共价键,[Zn(NH3)4]2+内存在配位键,水分子间存在范德华力和氢键,![]() 中存在共价键,综上,不存在的作用力是离子键,故答案为a;
中存在共价键,综上,不存在的作用力是离子键,故答案为a;
(4)ZnCl2,ZnBr2,ZnI2,组成与结构相似,在乙醇乙醚溶剂中能溶解,表明均为分子晶体,对于组成和结构相似的分子晶体,随着相对分子质量的增加,范德华力增强,熔沸点也相应升高;
(5)①钾原子核电荷数为19,原子核外有19个电子,钾原子核外运动状态不同的电子数是19;
②晶胞中顶点钾原子和中心钾原子距离最近,且两个钾原子距离为acm,则晶胞的边长为![]() cm,晶胞的体积为
cm,晶胞的体积为![]() cm3,晶胞中K原子数目为8×
cm3,晶胞中K原子数目为8×![]() +1=2,晶胞的质量为
+1=2,晶胞的质量为![]() g,钾晶体的密度为
g,钾晶体的密度为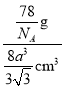 =
=![]() g/cm3。
g/cm3。