题目内容
【题目】某化学兴趣小组探究铝与稀盐酸反应速率的影响因素,用等质量的铝和等体积、等浓度的足量稀盐酸反应,得到的3组实验数据如下:
实验编号 | 铝的形状 | 反应温度/℃ | 收集100mLH2所需的时间 |
① | 铝粉 | 20 | 21 |
② | 铝片 | 20 | 82 |
③ | 铝片 | 30 | 35 |
回答下列问题:
(1)写出铝与稀盐酸反应的化学方程式______________________。
(2)探究温度对该反应速率影响的对比实验是③和_______ (填实验编号),得出的实验结论是________。
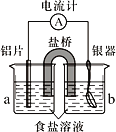
(3)若将该实验中“收集100mL H2所需时间改为“测量相同时间内生成H2的体积”,可选用的排水量气装置为下图中的______________(填装置代号)。

【答案】2Al+6HCl=2AlCl3+3H2 ↑ ② 相同条件下,温度越高反应速率越快 a
【解析】
从表中可以看出,探究铝与稀盐酸反应速率的影响因素,实验探究的内容有两个:一个是探究铝的形状对反应速率的影响,另一个是探究温度对反应速率的影响。需要注意的是,探究外界条件对反应速率的影响时,只能有一个自变量。所以,探究铝的形状对反应速率的影响时,应采用实验①②进行比较分析;探究温度对反应速率的影响时,应使用实验②③进行比较分析。
(1)铝与稀盐酸发生置换反应,生成氯化铝和氢气,化学方程式为2Al+6HCl=2AlCl3+3H2 ↑。答案为:2Al+6HCl=2AlCl3+3H2 ↑;
(2)探究温度对该反应速率影响时,铝的形状应相同,只有温度不同,所以对比实验是③和②;从实验中可以看出,温度高的实验,相同时间内产生的气体量多,由此得出的实验结论是相同条件下,温度越高反应速率越快。答案为:②;相同条件下,温度越高反应速率越快;
(3)在两个装置中,a装置中气体进入量筒,能排出量筒内的水,且排出水的体积等于生成气体的体积,而b装置是一个洗气装置,而不是排液法收集气体的装置,所以可选用的排水量气装置为图中的a。答案为:a。

 口算题天天练系列答案
口算题天天练系列答案