题目内容
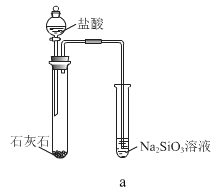
【题目】硅酸(H2SiO3)是一种难溶于水的弱酸,从溶液中析出时常形成凝胶状沉淀。实验室常用 Na2SiO3 溶液制备硅酸。某小组同学进行了如下实验:
编号 | Ⅰ | Ⅱ |
实验 |
|
|
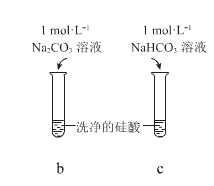
现象 | a 中产生凝胶状沉淀 | b 中凝胶状沉淀溶解,c 中无明显变化 |
下列结论不正确的是
A.Na2SiO3 溶液一定显碱性
B.由 Ⅰ 不 能 说 明 酸 性 H2CO3>H2SiO3
C.由Ⅱ可知,同浓度时 Na2CO3 溶液的碱性强于 NaHCO3 溶液
D.向 Na2SiO3 溶液中通入过量 CO2,发生反应:SiO32-+CO2+H2O=CO32-+H2SiO3↓
【答案】D
【解析】
A. Na2SiO3是强碱弱酸盐,在溶液中水解使溶液呈碱性,故A正确;
B.反应Ⅰ中盐酸与石灰石反应生成氯化钙、二氧化碳和水,盐酸具有挥发性,挥发出的氯化氢会干扰二氧化碳与硅酸钠的反应,不能确定碳酸的酸性强于硅酸,故B正确;
C. b中凝胶状沉淀溶解,c中无明显变化,说明同浓度的Na2CO3溶液的碱性强于NaHCO3溶液,故C正确;
D. Na2SiO3 溶液与过量 CO2反应生成硅酸白色胶状沉淀和碳酸氢钠,反应的离子方程式为SiO32-+CO2+2H2O=2HCO3-+H2SiO3↓,故D错误;
故选D。

【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
HCN | S8 | SF6 | B12结构单元 | |
结构模型 示意图 |
|
|
|
|
备注 | — | 易溶于CS2 | — | 熔点1 873 K |
A. HCN的结构式为H—C≡N,分子中含有2个σ键和2个π键
B. 固态硫S8属于原子晶体
C. SF6是由极性键构成的非极性分子
D. 单质硼属原子晶体,结构单元中含有30个B—B键
【题目】实验室用少量的溴和足量的乙醇制备1,2一二溴乙烷的装置如图所示:

有关数据列表如下:
乙醇 | 1.2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g/cm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
请按要求回答下列问题:
(1)写出A装置中的化学反应方程式_____;
(2)装置C中盛有氢氧化钠溶液,其作用是_____
(3)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____
(4)判断该制备反应已经结束的最简单方法是_____;
(5)若产物中有少量未反应的Br2,最好用_____洗涤除去;(填正确选项前的字母)
a 水 b 亚硫酸氢钠 c 碘化钠溶液 d 乙醇
(6)反应过程中应用冷水冷却装置D,其主要目的是_____;但又不能过度冷却(如用冰水),其原因是_____.