题目内容
对于A2+3B2  2C的反应来说,以下化学反应速率的表示中,反应速率最快的是 ( )
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是 ( )
A、v(B2)=0.8 mol·L-1·s-1
B、v(A2)=0.4 mol·L-1·s-1
C、v(C)=0.6 mol·L-1·s-1
D、v(B2)=4.2 mol·L-1·min-1
 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是 ( )
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是 ( )A、v(B2)=0.8 mol·L-1·s-1
B、v(A2)=0.4 mol·L-1·s-1
C、v(C)=0.6 mol·L-1·s-1
D、v(B2)=4.2 mol·L-1·min-1
B
试题分析:同一个化学反应,用不同的物质表示其反应速率时,速率数值可能不同,但表示的意义是相同的,所以比较反应速率快慢时,应该根据速率之比是相应的化学计量数之比先换算成用同一种物质表示,然后才能直接比较速率数值。根据反应式可知,如果都用B2表示反应速率则分别是(mol·L-1·s-1)0.8、1.2、0.9、0.07,所以反应速率最快的是选项B,答案选B。

练习册系列答案
相关题目

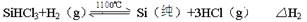
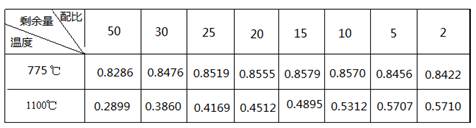
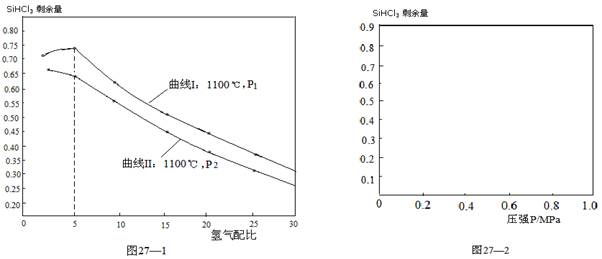
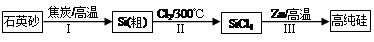
 Si(S)+2ZnCl2(l) △H1<0
Si(S)+2ZnCl2(l) △H1<0 4NO(g)+6HO(g) △H=-Q kJ· mol-1(Q>0),容器内部分物质的物质的量浓度如下表:
4NO(g)+6HO(g) △H=-Q kJ· mol-1(Q>0),容器内部分物质的物质的量浓度如下表: 2C(g)+2D(g),在不同条件下的化学反应速率,其中反应速率最快的是( )
2C(g)+2D(g),在不同条件下的化学反应速率,其中反应速率最快的是( )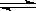 Z 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是 ( )
Z 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是 ( ) 
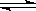 2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )。
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )。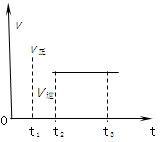
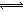 HOI(aq) △H2
HOI(aq) △H2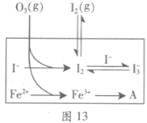
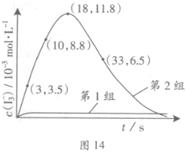
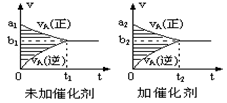
 pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下右图:①a1>a2②a1<a2③b1>b2④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下右图:①a1>a2②a1<a2③b1>b2④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是