题目内容
【题目】在20 L的密闭容器中按物质的量之比1∶2充入CO和H2,发生反应CO(g)+2H2(g)CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO的变化如图所示,p2和195 ℃时n(H2)随时间的变化结果如下表所示。下列说法正确的是( )
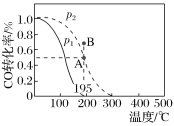
p2和195 ℃时n(H2)
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 5 | 4 | 4 |
A.p2和195 ℃时,0~3 min,反应速率v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
B.p1<p2,ΔH>0
C.195 ℃、p2时,在B点:v正>v逆
D.在p2和195 ℃时,该反应的平衡常数为25
【答案】D
【解析】
A.0~3min,Δn(H2)=4mol,Δc(H2)=![]() =0.2 mol·L-1,v(H2)=
=0.2 mol·L-1,v(H2)=![]() ,v(H2) :v(CH3OH)=2:1,则v(CH3OH)≈0.033 mol·L-1·min-1,故A错误;
,v(H2) :v(CH3OH)=2:1,则v(CH3OH)≈0.033 mol·L-1·min-1,故A错误;
B.由任意一条曲线知,随温度升高,CO转化率减小,故ΔH<0,由于增大压强时,平衡右移,故p1<p2,故B错误;
C.从B点到A点,CO转化率减小,反应向左进行,故v正<v逆,故C错误;
D.达到平衡时,CO、H2、CH3OH的平衡浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.1 mol·L-1,则平衡常数K=![]() =
=![]() =
=![]() =25,故D正确;
=25,故D正确;
答案选D。

【题目】根据杂化轨道理论和价电子对互斥理论模型判断,下列分子或离子的中心原子杂化方式及空间构型正确的是( )
选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥理论模型 | 分子或离子的空间构型 |
A | H2O | sp1 | 直线形 | 直线形 |
B | BBr3 | sp2 | 平面三角形 | 三角锥形 |
C | PCl3 | sp2 | 四面体形 | 平面三角形 |
D | CO32- | sp2 | 平面三角形 | 平面三角形 |
A.AB.BC.CD.D
【题目】有机物的结构可用键线式表示,如:
结构简式 |
|
|
|
键线式 |
|
|
|
(1)![]() 的分子式为___________。
的分子式为___________。
(2)已知三个乙炔分子反应生成苯,试写出三个丙炔分子反应生成的芳香烃分子的键线式:__________(填一种即可)。
(3)由![]() 以及必要的无机试剂可合成
以及必要的无机试剂可合成 ,写出第一步合成反应的化学方程式:________。
,写出第一步合成反应的化学方程式:________。
(4)A为![]() 的一种同分异构体,A的一氯代物有三种,且A与
的一种同分异构体,A的一氯代物有三种,且A与![]() 按物质的量之比为
按物质的量之比为![]() 加成得到的产物只有一种(不考虑顺反、立体异构),则A可能的结构简式有_____________。
加成得到的产物只有一种(不考虑顺反、立体异构),则A可能的结构简式有_____________。