题目内容
【题目】有一包白色粉末,其中可能含有KCl、Ba(NO3)2、CuSO4、Na2CO3,现通过以下实验流程进行检验(假设物质间的反应恰好完全)。回答下列问题:
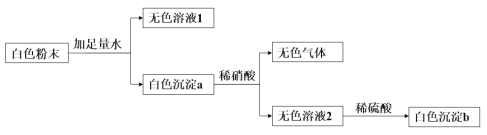
(1)白色粉末中一定没有的物质是_____________(填化学式,下同)。
(2)无色溶液1中一定含有的溶质___________,是可能含有的溶质是___________。
(3)生成无色气体的化学方程式为__________________________________;该反应属于____________(填反应基本类型).
(4)生成白色沉淀b的离子方程式为__________________________________ 。
【答案】CuSO4 NaNO3 KCl BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑ 复分解反应 Ba2++SO42-=BaSO4↓
【解析】
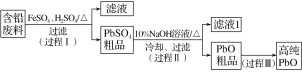
白色粉末加入水中,振荡,有白色沉淀a生成,过滤后溶液1呈无色,说明不含CuSO4;向沉淀a中加入足量稀硝酸,固体完全溶解,并有气泡产生,应为碳酸钡沉淀,说明含有Ba(NO3)2和Na2CO3,生成的气体为CO2;无色溶液2中滴入稀硫酸,有白色沉淀b产生,此沉淀为BaSO4,以此解答该题。
白色粉末加入水中,振荡,有白色沉淀a生成,过滤后溶液1呈无色,说明不含CuSO4;向沉淀a中加入足量稀硝酸,固体完全溶解,并有气泡产生,应为碳酸钡沉淀,说明含有Ba(NO3)2和Na2CO3,生成的气体为CO2;无色溶液2中滴入稀硫酸,有白色沉淀b产生,此沉淀为BaSO4,说明粉末中一定含有Ba(NO3)2和Na2CO3,一定没有CuSO4,可能有KCl;
(1)白色粉末中一定没有的物质是CuSO4;
(2) 粉末中一定含有Ba(NO3)2和Na2CO3,可能有KCl,则无色溶液1中一定含有的溶质是NaNO3,是可能含有的溶质是KCl;
(3)碳酸钡溶于稀硝酸生成CO2气体发生反应的化学方程式为BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑;该反应属于复分解反应;
(4)白色沉淀b为BaSO4,反应的离子方程式为Ba2++SO42-=BaSO4↓。

【题目】下列实验结论与实验现象相符合的一组是
选项 | 实验 | 现象 | 结论 |
A | 向某盐溶液中加入浓NaOH溶液,加热 | 产生的气体能使湿润的红色石蕊试纸变蓝 | 原溶液中含有 |
B | 把SO2通入紫色的酸性高锰酸钾溶液中 | 溶液紫色褪去 | SO2具有漂白性 |
C | 向蔗糖中滴加浓硫酸 | 蔗糖变黑 | 浓硫酸具有吸水性 |
D | 向盛有Cu片的试管中加入稀H2SO4,无明显现象,再加入NaNO3固体 | Cu片逐渐溶解,产生气 泡,溶液变蓝 | NaNO3是催化剂,可增大Cu与稀H2SO4反应的化学反应速率 |
A.AB.BC.CD.D