题目内容
【题目】高一学生小强的化学笔记中有如下内容,你认为他的笔记中有几处错误( )
①依据水溶液能否导电将物质分为电解质与非电解质
②单质可分为金属单质和非金属单质
③化合物主要包括:酸、碱、盐和氧化物
④按照分散剂粒子直径大小可将分散系分为溶液、浊液和胶体
⑤溶液呈电中性,胶体带有电荷
A.二处B.三处C.四处D.五处
【答案】B
【解析】
①依据水溶液或熔融状态能否导电将化合物分为电解质与非电解质,①错误;
②单质可分为金属单质和非金属单质,②正确;
③无机化合物主要包括:酸、碱、盐和氧化物,③错误;
④按照分散剂粒子直径大小可将分散系分为溶液、浊液和胶体,④正确;
⑤溶液呈电中性,胶体不带电,胶体粒子带电荷,⑤错误;
有3处错误,故选B。

 阅读快车系列答案
阅读快车系列答案【题目】某实验小组用 0.50 mol/L NaOH 溶液和 0.50 mol/L 硫酸溶液在如下图所示的装置中 进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
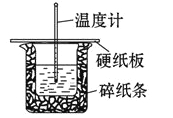
(1)从实验装置上看,图中缺少的一种玻璃仪器是_____。
(2)烧杯间填满碎纸条的作用是_____。
(3)若大烧杯上不盖硬纸板,求得的反应热数值______填“偏大”“偏小”或“无影响”)。
(4)若取取 50 mL NaOH 溶液和 30 mL 硫酸溶液进行实验,实验数据如下表。
温度 实验次数 | 起始温度 t1/℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 30.1 |
2 | 27.0 | 27.4 | 27.2 | 33.3 |
3 | 25.9 | 25.9 | 25.9 | 29.8 |
4 | 26.4 | 26.2 | 26.3 | 30.4 |
近似认为 0.50 mol/L NaOH 溶液和 0.50 mol/L 硫酸溶液的密度都是 1 g/cm3,中和后生成溶液 的比热容 c=4.18 J/(g·℃)。则中和热△H=_____(取小数点后一位)。
【题目】下列关于纯净物、混合物、电解质、非电解质的正确组合为()
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 盐酸 | 冰水混合物 | 硫酸 | 干冰 |
B | 蒸馏水 | 蔗糖溶液 | 硫酸钡 | 二氧化硫 |
C | 胆矾 | 盐酸 | 铁 | 乙醇 |
D | 碘酒 | 食盐水 | 氯化铜 | 碳酸钙 |
A.AB.BC.CD.D