题目内容
下列离子方程式书写正确的是( )
A.过量的SO2通入NaOH溶液中:SO2+2OH-=SO +H2O +H2O |
| B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
C.NaNO2溶液中加入酸性KMnO4溶液:2MnO +5NO +5NO +6H+=2Mn2++5NO +6H+=2Mn2++5NO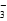 +3H2O +3H2O |
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO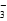 +Ba2++2OH-=BaCO3↓+2H2O+CO +Ba2++2OH-=BaCO3↓+2H2O+CO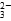 |
C
解析

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
下列方程式中正确的是
| A.FeCl2溶液滴加碘水:2Fe2++I2=2Fe3++2I— |
| B.双氧水中滴加2滴FeCl3溶液:2Fe3++H2O2=2Fe2++O2↑+2H+ |
| C.双氧水加入稀硫酸和KI溶液: H2O2+2H++2I—= I2+ O2↑+2 H2O |
| D.在Mg(OH)2悬浊液中滴加氯化铵溶液:Mg(OH)2+2NH4Cl=2NH3·H2O+MgCl2 |
下列反应的离子方程式正确的是 ( )
| A.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2 = 2Fe3++Br2+4Cl- |
| B.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++2OH-+NH4++HCO3- = BaCO3↓+NH3·H2O+H2O |
| C.氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| D.过量CO2通入氢氧化钠溶液中 CO2+2OH- = CO32-+H2O |
下列有关判断正确的是( )
| A.0.1mol/LNa2CO3溶液:c(OH-)= 2c(H2CO3)+ c(HCO3-)+ c(H+) |
| B.能使紫色石蕊试液呈红色的溶液:Na+、NH、I-、NO可以大量共存 |
| C.任何条件下,pH=13的氢氧化钠溶液中:c(OH-)=0.1mol/L |
| D.NH4HCO3溶于过量的NaOH溶液中:HCO3-+ OH-= CO32- + H2O |
下列相关反应的离子方程式书写正确的是
| A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B.硫酸铜溶液显酸性:Cu2++2H2O=Cu(OH)2↓+2H+ |
C.向碳酸氢铵溶液中加过量石灰水并加热: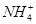 +OH-=NH3↑+H2O +OH-=NH3↑+H2O |
D.用酸化的高锰酸钾溶液氧化双氧水:2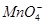 +6H++5H2O2=2Mn2++5O2↑+8H2O +6H++5H2O2=2Mn2++5O2↑+8H2O |
下列表示对应化学反应的离子方程式正确的是
| A.用氨水溶解氯化银沉淀:Ag++2 NH3·H2O=[Ag(NH3)2]++2H2O |
| B.二氧化硫通入氯化铁溶液:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+ |
| C.硫酸氢铵溶液中滴加少量NaOH溶液:H++NH4++2OH-=NH3·H2O+H2O |
| D.碱性条件下铝粉还原NaNO2:NO2-+2Al+3OH-+H2O=2AlO2-+NH3·H2O |
常温下,在指定环境中,下列各组离子一定可以大量共存的是( )。
| A.使pH试纸呈红色的溶液中:Fe2+、ClO-、SO42-、Na+ |
| B.在pH=3的溶液中:Na+、NO3-、Cl-、Al3+ |
| C.由水电离出的c(H+)=10-13 mol·L-1的溶液中:CO32-、SO42-、Cl-、Na+ |
| D.加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- |
下列叙述中正确的是 ( )。
| A.物质的溶解过程,实质上就是其电离过程 |
| B.三氧化硫的水溶液能导电,所以三氧化硫是电解质 |
| C.1 L 0.1 mol·L-1的H2SO4溶液中含有0.2 mol H+ |
| D.1 L 0.1 mol·L-1的H2SO3溶液中含有0.2 mol H+ |
下列对实验现象的预测不正确的是( )
| A.向Na2SiO3溶液中通入CO2,溶液变浑浊,继续通入CO2至过量,浑浊消失 |
| B.向Na2CO3饱和溶液中通入CO2,溶液变浑浊,继续通入CO2,有晶体析出 |
| C.向Ca(ClO)2溶液中通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 |
| D.向Ca(OH)2溶液中通入CO2,溶液变浑浊,继续通入CO2至过量,浑浊消失,再加入过量NaOH溶液,溶液又变浑浊 |