题目内容
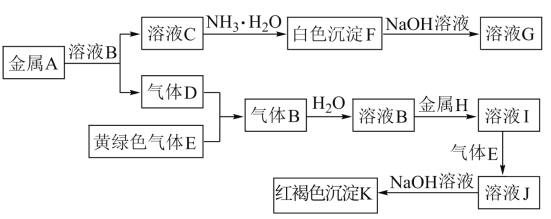
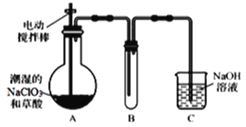
【题目】ClO2气体是一种高效、广谱、安全的杀菌消毒剂,可用NaClO3和草酸(H2C2O4)反应制得。无水草酸100℃可以升华。某学习小组用下图装置模拟工业制取收集ClO2 。
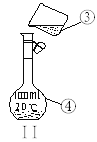
(1)实验时装置A需在60℃~100℃进行的原因是_________,控制所需温度的方法是________。
(2)装置A中反应产物有Na2CO3、ClO2和CO2等,该反应的化学方程式为___________。
(3)在装置C中ClO2和NaOH反应生成等物质的量的两种盐,其中一种盐为NaClO2 ,写出反应的离子方程式_________________。
【答案】温度过低,化学反应速率较慢,温度过高草酸升华或分解 水浴加热 2NaClO3+H2C2O4![]() Na2CO3+CO2↑+2ClO2↑+H2O 2ClO2+2OH-=ClO3-+ClO2-+H2O
Na2CO3+CO2↑+2ClO2↑+H2O 2ClO2+2OH-=ClO3-+ClO2-+H2O
【解析】
装置A中盛放草酸和NaClO3,反应生成ClO2气体,发生2NaClO3+H2C2O4 ![]() Na2CO3+CO2↑+2ClO2↑+H2O,装置A用电动搅拌棒,将反应物充分混合(或充分反应、或使反应物受热均匀),B为ClO2的凝集装置,装置C为尾气吸收装置。
Na2CO3+CO2↑+2ClO2↑+H2O,装置A用电动搅拌棒,将反应物充分混合(或充分反应、或使反应物受热均匀),B为ClO2的凝集装置,装置C为尾气吸收装置。
(1)一般来说,升高温度,活化分子的百分数增大,反应速率增大,温度过低,化学反应速率较慢,无水草酸100℃可以升华,温度过高草酸升华或分解,所以实验时装置A需在60℃~100℃进行,反应温度低于水的沸点,用水浴可使反应容器受热均匀,所以反应要用水浴加热;
(2)装置A中反应物为NaClO3、H2C2O4,产物有Na2CO3、ClO2和CO2等,方程式为2NaClO3+H2C2O4![]() Na2CO3+CO2↑+2ClO2↑+H2O;
Na2CO3+CO2↑+2ClO2↑+H2O;
(3)NaOH吸收ClO2尾气,生成物质的量之比为1:1的两种阴离子,一种为ClO2-,氧化还原反应规律,另一种离子中Cl元素化合价升高,即为ClO3-,反应的离子方程式为:2ClO2+2OH-=ClO3-+ClO2-+H2O。

【题目】某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡,混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案:
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
浓度(mol/L) | 体积/mL | 浓度(mol/L) | 体积/mL | ||
① | 0.10 | 2.0 | 0.01 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.01 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.01 | 4.0 | 50 |
(1)已知反应后H2C2O4转化为CO2逸出,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:n(H2C2O4)∶n(KMnO4) ______________。
(2)探究温度对化学反应速率影响的实验编号是_______ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是 ________.
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=_______。