题目内容
【题目】工业尾气中的氮氧化物常用氨催化吸收法,原理是NH3与NOx反应生成无毒物质。某同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。
(一)提供的装置
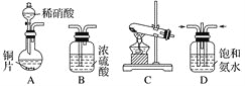

(二)NH3的制取
(1)下列有关实验室制备气体的说法正确的是__________(填序号)。
①可以用排饱和食盐水的方法收集氯气 ②用赤热的炭与水蒸气反应制取氢气 ③实验室制氧气有时需要加热,有时不需要加热 ④用无水氯化钙干燥氨气 ⑤用浓盐酸洗涤高锰酸钾分解制氧气的试管
(2)从所提供的装置中选取一个能制取氨气的装置:________________(填序号)。
(3)当采用你所选用的装置制取氨气时,相应反应的化学方程式是___________。
(三)模拟尾气的处理
选用上述部分装置,按下列顺序连接成模拟尾气处理装置,回答有关问题:

(4)A中反应的离子方程式为___________。
(5)D装置中的液体可换成________(填序号)。
a CuSO4 b H2O c CCl4 d 浓硫酸
(6)该同学所设计的模拟尾气处理实验还存在的明显缺陷是________________。
【答案】①③⑤ C或G 2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O或CaO+NH3·H2O=NH3↑+Ca(OH)2(要对应) 3Cu+2NO3+8H+=3Cu2++2NO↑+4H2O c NO尾气直接排放,没有进行处理
2NH3↑+CaCl2+2H2O或CaO+NH3·H2O=NH3↑+Ca(OH)2(要对应) 3Cu+2NO3+8H+=3Cu2++2NO↑+4H2O c NO尾气直接排放,没有进行处理
【解析】
(1)①氯气在饱和食盐水中的溶解度较小,可以用排饱和食盐水的方法收集氯气,①正确;
②用赤热的炭与水蒸气反应生成CO、H2,制取的氢气含有杂质,②错误;
③实验室制氧气,用高锰酸钾或氯酸钾时需要加热,用过氧化氢时不需要加热,③正确;
④氯化钙与氨气可形成配合物,不能用无水氯化钙干燥氨气,④错误;
⑤用高锰酸钾制取氧气后剩余的固体为二氧化锰、高锰酸钾,均可与浓盐酸反应生成可溶性的二氯化锰,故可用浓盐酸洗涤高锰酸钾分解制氧气的试管,⑤正确;
故答案为:①③⑤;
(2)实验室制备氨气可用氢氧化钙与氯化铵固体加热法,也可以用浓氨水与氢氧化钠(或氧化钙)在常温下制取。可选装置C或G,故答案为:C或G;
(3)根据所选装置,相应制备氨气的化学方程式为2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O或CaO+NH3·H2O=NH3↑+Ca(OH)2(要对应),故答案为:2NH4Cl+Ca(OH)2
2NH3↑+CaCl2+2H2O或CaO+NH3·H2O=NH3↑+Ca(OH)2(要对应),故答案为:2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O或CaO+NH3·H2O=NH3↑+Ca(OH)2;
2NH3↑+CaCl2+2H2O或CaO+NH3·H2O=NH3↑+Ca(OH)2;
(4)A中为Cu与稀硝酸的反应:3Cu+2 NO3+8H+=3Cu2++2NO↑+4H2O,故答案为:3Cu+2 NO3+8H+=3Cu2++2NO↑+4H2O;
(5)D中用饱和氨水防止氨气被吸收,因此还可以换成CCl4,故答案为:c;
(6)该反应中尾气含有NO等污染性气体,应除去后再排空,故答案为:NO尾气直接排放,没有进行处理。

【题目】一定温度下,体积为2 L的密闭容器中X、Y、Z三种气体的初始物质的量和平衡物质的量如下表:
物质 | X | Y | Z |
初始物质的量(mol) | 0.2 | 0.2 | 0 |
平衡物质的量(mol) | 0.1 | 0.05 | 0.1 |
下列说法正确的是( )
A. 反应可表示为2X+3Y![]() 2Z,其平衡常数为8 000
2Z,其平衡常数为8 000
B. 增大压强使平衡向生成Z的方向移动,平衡常数增大
C. 若将容器的体积压缩至1 L,则X的体积分数减小,浓度增大
D. 若升高温度时,Z的浓度增大,可知温度升高时正反应速率增大,逆反应速率 减小,平衡向正反应方向移动