��Ŀ����
����Ŀ�������£� HNO2�ĵ���ƽ�ⳣ��ΪK=4.6��10-4(��֪![]() �� ��20ml 0.01mol��L-1HNO2��Һ����μ�����ͬŨ�ȵ�NaOH��Һ����û��Һ��pH��NaOH��Һ����ı仯��ͼ��ʾ�������ж���ȷ����( )
�� ��20ml 0.01mol��L-1HNO2��Һ����μ�����ͬŨ�ȵ�NaOH��Һ����û��Һ��pH��NaOH��Һ����ı仯��ͼ��ʾ�������ж���ȷ����( )

A. X=20
B. a��b��c��d�ĵ��Ӧ����Һ��ˮ�ĵ���̶���С
C. a�����Һ��c(H+)=2.14��10-3mol��L-1
D. b����Һ����Ũ�ȵĴ�С��ϵΪc(HNO2)>c(Na+)>(NO2)
���𰸡�C
��������
HNO2�ĵ���ƽ�ⳣ��ΪK=4.6��10-4��������Ϊ������ڵ���ƽ�⣬���뷽��ʽΪHNO2NO2-+H+��
A.��20mL0��01molL-1��HNO2��Һ����μ�����ͬŨ�ȵ�NaOH��Һ����ǡ�÷�Ӧ��Ҫ����������Һ���20ml��������NaNO2������Ϊ����ǿ���Σ���ˮ��ʹ��Һƫ���ԣ���c������Һ�����ԣ�����X��20mL����A����ȷ��
B.c������Һ�����ԣ�����ΪHNO2��NaNO2�����Һ������������Һ���Ϊ20mlʱǡ�÷�Ӧ����ô��a��ʼ��ǡ����ȫ��Ӧʱ��ˮ�ĵ���̶�������d���ͼ�ж���������ǡ�÷�Ӧ֮ǰ����ǡ�÷�Ӧ֮��B����ȷ��
C.��HNO2NO2-+H+�� ![]() ��
��![]() ���õ�c(H+)=2.14��10-3mol��L-1����C��ȷ��
���õ�c(H+)=2.14��10-3mol��L-1����C��ȷ��
D.b����ҺΪHNO2��NaNO2�����Һ����Ũ�ȱ�Ϊ1��1����NO2-+H2OHNO2+OH-��HNO2H++NO2-����Ϊ��Һ�����ԣ����Ե���̶ȴ���ˮ��̶ȣ�����Ũ�ȴ�СΪc(NO2-)��c(Na+)��c(HNO2)����D����ȷ��
�𰸣�C

 ����������ϵ�д�
����������ϵ�д�����Ŀ��Bodensteins�о���ӦH2(g)��I2(g)![]() 2HI(g)���¶�ΪTʱ�������������Ϊ1 L���ܱ������н���ʵ�飬������������е⻯������ʵ�������w (HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
2HI(g)���¶�ΪTʱ�������������Ϊ1 L���ܱ������н���ʵ�飬������������е⻯������ʵ�������w (HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
������� | ��ʼ���� | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
I | 0.5 mol I2��0.5 mol H2 | w (HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
II | x mol HI | w (HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
�о�����������Ӧ�У�v����ka��w(H2)��w(I2)��v����kb��w2(HI)������ka��kbΪ����������˵����ȷ���ǣ�
A. �¶�ΪTʱ���÷�Ӧ![]()
B. ����I����ǰ20 min��ƽ������v(HI)=0.0125 mol��L��1��min��1
C. ����ʼʱ������I�м������ʵ�����Ϊ0.1 mol��H2��I2��HI����Ӧ�������
D. ���������д���ka��= ka����kb��= kb������x��ֵ����Ϊ�κ�ֵ
����Ŀ���о���ѧ��Ӧʱ����Ҫ�������ʱ仯�������仯����Ҫ��ע��Ӧ�Ŀ������ȡ��ش��������⣺
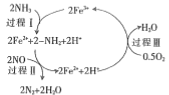
(1)NH3��ԭNO����Ҫ�����������������䷴Ӧ������������ϵ����ͼ��ʾ��

����ͼ����Ϊ�ı��˷�Ӧ��������Ӧ�Ļ��b___________(���������������)a��
��������Ӧ���Ȼ�ѧ����ʽ�ɱ�ʾΪ��Ӧ�����������H��___________(��E1�� E2�Ĵ���ʽ��ʾ)
���о����֣�һ�������µ�������Ӧ���̿�����ͼ��ʾ������������ԭ��Ӧ�����ʵ����ã�NOΪ��____�������ܷ�Ӧ�Ļ�ѧ����ʽΪ��___________��
(2)һ���¶��£�����ͬ���ʵ�����H2O(g)��CO�ֱ�ͨ���ݻ�Ϊ1L�ĺ����ܱ������У����з�ӦH2O(g)+CO(g)��CO2(g)+H2(g)���õ������ʾ���������ݣ�
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
H2O(g) | CO(g) | CO(g) | H2(g) | |||
1 | 650 | 2.0 | 4.0 | 3.0 | 1.0 | 5 |
2 | 900 | 1.0 | 2.0 | 1.8 | 0.2 | 4 |
3 | 900 | a | b | c | d | t |
��ʵ��2��4min
��650��ʱ�����ڴ������г���2.0molH2O(g)��1.0molCO(g)��1.0molCO2(g)��xmolH2(g)��Ҫʹ��Ӧ�ڿ�ʼʱ��������Ӧ������У���xӦ�����������___________��
����a=2.0��b=1.0����ƽ��ʱʵ��2��H2O(g)��ʵ��3��CO(g)��ת����(��)�Ĺ�ϵΪ��(H2O)___________(�������������=��)��(CO)��


