题目内容
18.计算在标准状况下2mol NH3的体积是44.8L;在标准状况下,某气体的密度是H2密度的16倍,则该气体的摩尔质量是32g/mol.分析 根据V=nVm计算,气体的密度之比等于摩尔质量之比.
解答 解:在标准状况下2mol NH3的体积是V=nVm=2mol×22.4L/mol=44.8L;
在标准状况下,某气体的密度是H2密度的16倍,氢气的摩尔质量为2g/mol,气体的密度之比等于摩尔质量之比,则该气体的摩尔质量是2g/mol×16=32g/mol;
故答案为:44.8L;32g/mol.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关计算公式,有利于基础知识的巩固.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
8.下列哪个选项属于碳链异构( )
| A. | CH3CH2 CH2CH3和CH3CH(CH3)2 | B. | CH2=C(CH3)2和CH3CH=CHCH3 | ||
| C. | CH3CH2OH和CH3OCH3 | D. | CH3CH2 CH2COOH 和CH3COOCH2CH3 |
6.分别滴加下列试剂后,试管中的溶液颜色变红的是( )
| A. | 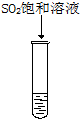 品红溶液 | B. | 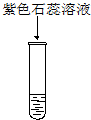 氨水 | C. | 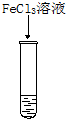 KSCN溶液 | D. | 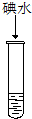 淀粉溶液 |
3.下列关于物质分类的说法正确的是( )
| A. | 牛奶、有色玻璃都属于胶体 | |
| B. | 漂白粉、石英都属于纯净物 | |
| C. | 氯化铵、次氯酸都属于强电解质 | |
| D. | 葡萄糖、蛋白质都属于高分子化合物 |

