题目内容
下列实验操作或现象分析正确的是( )
A、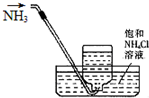 收集氨气 |
B、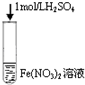 管口出现还原产物NO2红棕色气体 |
C、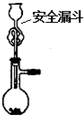 制取二氧化硫 |
D、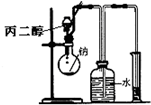 测定丙二醇的分子结构 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.氨气极易溶于水,不能用排水溶液的方法收集;
B.亚铁离子和稀硝酸反应生成NO,NO易被氧气氧化;
C.安全漏斗能起到液封的作用;
D.该实验利用排水法收集氢气,只能确定丙二醇中的官能团个数.
B.亚铁离子和稀硝酸反应生成NO,NO易被氧气氧化;
C.安全漏斗能起到液封的作用;
D.该实验利用排水法收集氢气,只能确定丙二醇中的官能团个数.
解答:
解:A.氨气极易溶于水,虽然氯化铵中含有铵根离子抑制部分氨气溶解,但氨气的溶解度仍然很大,所以不能用排氯化铵溶液的方法收集氨气,应该采用向下排空气法收集,故A错误;
B.加入稀硫酸后,酸性条件下,硝酸根离子具有强氧化性,能将亚铁离子氧化为铁离子,自身被还原为NO,NO不稳定,被氧气氧化生成二氧化氮,所以管口出现还原产物NO2红棕色气体是二次还原产物,而不是亚铁离子和硝酸反应的直接产物,故B错误;
C.实验室用浓硫酸和亚硫酸钠混合制取二氧化硫,所以该装置属于固液混合不加热型装置,安全漏斗能起到液封的作用,所以生成的气体不能通过漏斗逸出,故C正确;
D.该实验利用排水法收集氢气,只能确定丙二醇中的官能团个数,不能确定其结构,可以利用红外光谱、核磁共振氢谱等方法确定丙二醇结构,故D错误;
故选C.
B.加入稀硫酸后,酸性条件下,硝酸根离子具有强氧化性,能将亚铁离子氧化为铁离子,自身被还原为NO,NO不稳定,被氧气氧化生成二氧化氮,所以管口出现还原产物NO2红棕色气体是二次还原产物,而不是亚铁离子和硝酸反应的直接产物,故B错误;
C.实验室用浓硫酸和亚硫酸钠混合制取二氧化硫,所以该装置属于固液混合不加热型装置,安全漏斗能起到液封的作用,所以生成的气体不能通过漏斗逸出,故C正确;
D.该实验利用排水法收集氢气,只能确定丙二醇中的官能团个数,不能确定其结构,可以利用红外光谱、核磁共振氢谱等方法确定丙二醇结构,故D错误;
故选C.
点评:本题考查了化学实验方案评价,涉及较综合,明确实验原理是解本题关键,易错选项是B,注意:酸性条件下,硝酸根离子能氧化亚铁离子,中性或碱性条件下不能氧化亚铁离子.

练习册系列答案
相关题目
下列各组物质中,所含化学键类型完全相同的是( )
| A、HCl和MgCl2 |
| B、H2O和CO2 |
| C、Ar和CCl4 |
| D、NH4Cl和NaOH |
可逆反应mA(g)+nB?pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是( )
| A、若增加B的量,平衡体系颜色加深,说明B必是气体 |
| B、增大压强,平衡不移动,说明m+n一定等于p+q |
| C、升高温度,A的转化率减小,说明正反应是吸热反应 |
| D、若B是气体,增大A的量,A、B的转化率都增大 |
化学与生产、生活、社会密切相关,下列说法正确的是( )
| A、煤经气化和液化两个物理过程后可变为清洁能源,这是煤综合利用的主要方法 |
| B、蛋白质、淀粉、纤维素、油脂等都能在人体内水解并提供能量 |
| C、利用风能发电、使用太阳能热水器、应用无氟制冷剂均有利于降低大气中的二氧化碳 |
| D、积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料 |
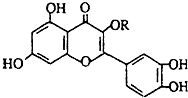 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A、1mol维生素P在一定条件下最多可以和7mol H2反应 |
| B、分子中共有两个苯环 |
| C、维生素P能与FeCl3溶液发生显色反应 |
| D、1mol维生素P可以和4mol NaOH反应 |
21世纪是钛的世纪.在800℃~1000℃时电解TiO2可制得钛,装置如图所示.下列叙述正确的是( )


| A、a为电源的正极 |
| B、石墨电极上发生还原反应 |
| C、阴极发生的反应为:TiO2+4e-═Ti+2O2- |
| D、每生成0.1mol钛,转移电子0.2mol |
下列叙述不正确的是( )
| A、NH3易液化,氨常用作制冷剂 |
| B、NH4Cl中有少量的I2:通过加热的方法除去 |
| C、铵盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处 |
| D、浓硝酸需保存在棕色瓶中 |
