题目内容
可逆反应mA(g)+nB?pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是( )
| A、若增加B的量,平衡体系颜色加深,说明B必是气体 |
| B、增大压强,平衡不移动,说明m+n一定等于p+q |
| C、升高温度,A的转化率减小,说明正反应是吸热反应 |
| D、若B是气体,增大A的量,A、B的转化率都增大 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:升高温度、增大压强、增大反应物浓度、使用催化剂都会使正反应速率增大,结合平衡移动原理分析平衡移动的可能方向,据此解答.
解答:
解:A、若增加B的量,平衡正向移动,削弱B的浓度,但未抵消,平衡体系B的浓度变大,颜色加深,说明B必是气体,故A正确;
B、如D是非气体,则是说明m+n等于p,故B错误;
C、升高温度,A的转化率减小,说明平衡逆向移动,逆反应是吸热反应,故C错误;
D、若B是气体,增大A的量,A的转化率减小,B的转化率增大,故D错误;
故选A.
B、如D是非气体,则是说明m+n等于p,故B错误;
C、升高温度,A的转化率减小,说明平衡逆向移动,逆反应是吸热反应,故C错误;
D、若B是气体,增大A的量,A的转化率减小,B的转化率增大,故D错误;
故选A.
点评:本题考查了影响化学平衡的因素,难度不大,易错选项是B,注意固体和纯液体改变用量对反应速率无影响,催化剂只影响反应速率不影响平衡的移动.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
已知反应:2M(g)+N(g)+P(g)
2Q(g)+3R(g)△H>0,在恒容的密闭容器中,下列有关说法正确的是( )
| 180℃ |
| 催化剂 |
| A、平衡时,其他条件不变,增加M的浓度,N的转化率减小 |
| B、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| C、单位时间内消耗N和Q的物质的量比为1:1时,反应达到平衡 |
| D、其他条件不变,使用高效催化剂,N和P的转化率增大 |
NA为阿伏加德罗常数,下列叙述错误的是( )
| A、0.1mol Na2O2与足量水完全反应时,转移电子数目为0.1NA |
| B、12g金刚石含有的共价键数为2NA |
| C、0.1mol的铜与足量的浓硫酸反应生成SO2的体积(标况)约为2.24L |
| D、在1L 0.1mol?L-1碳酸钠溶液中阴离子总数小于0.1NA |
下列除杂方法正确的是( )
①除去乙烷中少量的乙烯:通入H2,加催化剂反应
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液
③除去苯中少量的苯酚:滴加适量溴水,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去苯中少量的甲苯:加足量KMnO4溶液,分液.
①除去乙烷中少量的乙烯:通入H2,加催化剂反应
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液
③除去苯中少量的苯酚:滴加适量溴水,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去苯中少量的甲苯:加足量KMnO4溶液,分液.
| A、①②③ | B、②③④ |
| C、②④⑤ | D、③④⑤ |
下列实验操作或现象分析正确的是( )
A、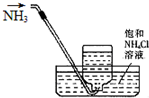 收集氨气 |
B、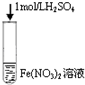 管口出现还原产物NO2红棕色气体 |
C、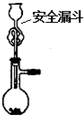 制取二氧化硫 |
D、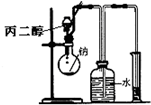 测定丙二醇的分子结构 |
下列实验不能达到实验目的是( )
①实验窒用无水乙醇和浓硫酸共热到140℃即可制取乙烯
②验证R-X是碘代烷,把R-X与NaOH水溶液混合加热,再往其中加入硝酸银溶液即可
③做醛的还原性实验,向乙醛溶液中加入新制的Cu(OH)2悬浊液即可得到红色沉淀
④检验淀粉已水解,将淀粉与水和稀硫酸加热一段时间后,加入银氨溶液即可
⑤实验室制备乙酸乙酯,把乙醇和乙酸及稀硫酸溶液共热即可.
①实验窒用无水乙醇和浓硫酸共热到140℃即可制取乙烯
②验证R-X是碘代烷,把R-X与NaOH水溶液混合加热,再往其中加入硝酸银溶液即可
③做醛的还原性实验,向乙醛溶液中加入新制的Cu(OH)2悬浊液即可得到红色沉淀
④检验淀粉已水解,将淀粉与水和稀硫酸加热一段时间后,加入银氨溶液即可
⑤实验室制备乙酸乙酯,把乙醇和乙酸及稀硫酸溶液共热即可.
| A、①②③④⑤ | B、①③④ |
| C、①②③⑤ | D、②③⑤ |
某元素的最外层电子数为2,价电子数为5,并且是同族中原子序数最小的元素,关于该元素的判断错误的是( )
| A、电子排布式为1s22s22p63s23p63d34s2 |
| B、该元素为V |
| C、该元素为ⅡA族元素 |
| D、该元素位于d区 |