题目内容
下列有关元素的性质及其递变规律不正确的是( )
| A、短周期主族元素的最高正价等于其所在族序数,而O、F不符合该规律 |
| B、IA族与VIIA族的元素间形成共价化合物或离子化合物时,最外层都满足8e-结构 |
| C、VIIA族元素的简单阴离子还原性越强,对应氢化物的酸性越强,非金属性越弱 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.O、F没有正化合价;
B.氢化物及LiX不满足最外层都满足8e-结构;
C.VIIA族中非金属性越强,阴离子还原性越弱,非金属性越强,H-X键越稳定,氢化物的酸性越弱.
B.氢化物及LiX不满足最外层都满足8e-结构;
C.VIIA族中非金属性越强,阴离子还原性越弱,非金属性越强,H-X键越稳定,氢化物的酸性越弱.
解答:
解:A.短周期主族元素的最高正价等于其所在族序数,而O、F没有正化合价,不符合该规律,故A正确;
B.ⅠA族含H及碱金属元素,ⅦA族元素为卤素,氢化物HX中H原子不满足8电子结构,LiX中锂离子不满足8电子结构,故B错误;
C.VIIA族中阴离子还原性越强,元素的非金属性越弱,非金属性越强,H-X键越稳定,氢化物酸性越弱,故C正确;
故选B.
B.ⅠA族含H及碱金属元素,ⅦA族元素为卤素,氢化物HX中H原子不满足8电子结构,LiX中锂离子不满足8电子结构,故B错误;
C.VIIA族中阴离子还原性越强,元素的非金属性越弱,非金属性越强,H-X键越稳定,氢化物酸性越弱,故C正确;
故选B.
点评:本题考查元素周期律、化学键等,难度不大,侧重对基础知识的巩固,B选项中注意ⅠA族中H元素与Li元素结构特点.

练习册系列答案
相关题目
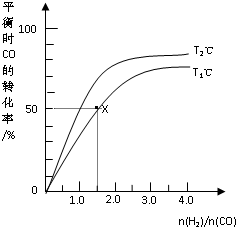 在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0.有关信息如图所示,下列说法正确的是( )
在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0.有关信息如图所示,下列说法正确的是( )| A、T1<T2 | ||
| B、T1℃时该反应的平衡常数为4.0 L2?mol-2 | ||
C、同一温度下,
| ||
D、相同条件下
|
把一块钠投入预先滴入2~3滴石蕊试液的水溶液中,可观察到的现象正确的一组为( )
①钠沉到水下面;②钠浮在水面上,四处游动;③钠熔成闪亮的小球,听到滋滋的响声;④溶液变红;⑤溶液变蓝.
①钠沉到水下面;②钠浮在水面上,四处游动;③钠熔成闪亮的小球,听到滋滋的响声;④溶液变红;⑤溶液变蓝.
| A、②③⑤ | B、①③④ |
| C、①③⑤ | D、②③④ |
下列物质间的反应肯定无明显实验现象的是( )
| A、新鲜的玫瑰花放置于盛有干燥的Cl2的集气瓶中 |
| B、少量CO2通入浓的BaCl2溶液中 |
| C、将新制的氯水逐滴滴入含有酚酞的烧碱溶液中 |
| D、未经打磨的铝片加入浓NaOH溶液中一段时间 |
下列化学药品与其危险化学品图形标志不一致的一组是( )
A、 烧碱--1 |
B、 甲烷--2 |
C、 酒精--3 |
D、 白磷--4 |
工业铁的冶炼的设备中是( )
| A、高炉 | B、接触室 |
| C、熔炉 | D、沸腾炉 |
下列关于Na2O2的叙述正确的是( )
| A、Na2O2晶体中的阴离子与阳离子的物质的量之比为1:1 |
| B、Na2O2为白色固体 |
| C、Na2O2应密闭保存于细口瓶中 |
| D、Na2O2与盐酸反应,不仅有盐和水生成,同时会放出无色气体 |
下列说法中正确的是( )
| A、元素周期表中元素排序的依据是元素的相对原子质量 |
| B、第IA金属比第IIA金属元素的金属性强 |
| C、元素周期表有十六个纵行,也就是十六个族 |
| D、元素周期表中元素排序的依据是原子的核电荷数 |