题目内容
下列关于Na2O2的叙述正确的是( )
| A、Na2O2晶体中的阴离子与阳离子的物质的量之比为1:1 |
| B、Na2O2为白色固体 |
| C、Na2O2应密闭保存于细口瓶中 |
| D、Na2O2与盐酸反应,不仅有盐和水生成,同时会放出无色气体 |
考点:钠的重要化合物
专题:元素及其化合物
分析:Na2O2为淡黄色固体,Na2O2具有强氧化性,可与水、二氧化碳反应生成氧气,Na2O2的电子式为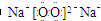 ,阴、阳离子的个数比为1:2,以此解答该题.
,阴、阳离子的个数比为1:2,以此解答该题.
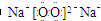 ,阴、阳离子的个数比为1:2,以此解答该题.
,阴、阳离子的个数比为1:2,以此解答该题.解答:
解:A.Na2O2的电子式为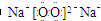 ,阴、阳离子的个数比为1:2,故A错误;
,阴、阳离子的个数比为1:2,故A错误;
B.Na2O2为淡黄色固体,故B错误;
C.固体药瓶因保存于广口瓶中,故C错误;
D.发生2Na2O2+4HCl+=4NaCl+O2↑+2H2O,故D正确.
故选D.
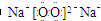 ,阴、阳离子的个数比为1:2,故A错误;
,阴、阳离子的个数比为1:2,故A错误;B.Na2O2为淡黄色固体,故B错误;
C.固体药瓶因保存于广口瓶中,故C错误;
D.发生2Na2O2+4HCl+=4NaCl+O2↑+2H2O,故D正确.
故选D.
点评:本题考查钠的重要化合物知识,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握过氧化钠与水、二氧化碳以及酸反应的特点,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
agCO2中含有b个分子,则阿伏加德罗常数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法中错误的是( )
| A、CO燃烧是放热反应 |
| B、浓硫酸在常温下能够使铁、铝等金属钝化 |
| C、CaO与H2O反应是吸热反应 |
| D、Na与NaCl在灼烧时火焰颜色相同 |
下列有关元素的性质及其递变规律不正确的是( )
| A、短周期主族元素的最高正价等于其所在族序数,而O、F不符合该规律 |
| B、IA族与VIIA族的元素间形成共价化合物或离子化合物时,最外层都满足8e-结构 |
| C、VIIA族元素的简单阴离子还原性越强,对应氢化物的酸性越强,非金属性越弱 |
下列说法正确的是( )
| A、冰和干冰既是纯净物又是化合物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| D、盐酸和食醋既是化合物又是酸 |
亚氯酸钠(NaClO2)可用作漂白剂,在酸性溶液中因生成亚氯酸而发生分解,分解的化学方程式为5HClO2=4ClO2↑+HCl+2H2O,ClO2是广谱型消毒剂.下列说法正确的是( )
| A、HClO2只是还原剂 |
| B、上述反应中,ClO2是氧化产物 |
| C、上述反应中,1mol HClO2分解转移2mol电子 |
| D、上述反应中,氧化剂与还原剂物质的量之比为1:4 |
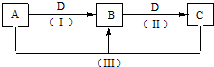 A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示.请回答下列问题:
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示.请回答下列问题: