题目内容
【题目】下列说法不正确的是
A.[Cu(NH3)4]SO4可通过CuSO4溶液与过量氨水作用得到
B.铁锈的主要成分可表示为Fe2O3·nH2O
C.钙单质可以从TiCl4中置换出Ti
D.可用H2还原MgO制备单质Mg
【答案】D
【解析】
A项、CuSO4溶液与少量氨水反应生成氢氧化铜沉淀,与过量氨水反应生成络合物[Cu(NH3)4]SO4,故A正确;
B项、铁在潮湿空气中发生吸氧腐蚀生成红棕色的铁锈,铁锈的主要成分可表示为Fe2O3·nH2O,故B正确;
C项、钙的化学性质活泼,在稀有气体的保护下,与熔融的四氯化钛反应可置换出Ti,故C正确;
D项、制备单质Mg应该用电解熔融MgCl2的方法,故D错误;
故选D。

练习册系列答案
相关题目
【题目】炼锌厂产生的工业废渣——锌渣(除了含Zn 外,还含有Fe、Al、Cd (镉)和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O 和金属镉(Cd)是一个有益的尝试,流程如下:
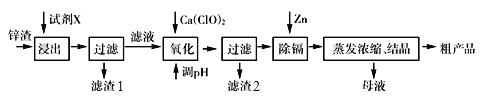
已知:金属活动性Zn> Cd
物质 | Fe(OH)3 | Al(OH)3 | Zn(OH)2 | Cd(OH)2 | Fe(OH)2 |
完全沉淀时的PH | ≥3.2 | ≥4.7 | ≥6.5 | ≥9.4 | ≥9.7 |
试回答下列问题:
(1)第一步浸出时用到的试剂X为__________,滤渣1的成分是___________。
(2)加入Ca(ClO)2 的目的是氧化Fe2+,写出反应的离子方程式____________________。
(3)调节pH 过程可以选用;本流程的pH 调节一般调至5,其目的是_____________________。
(4)写出过滤后加入过量的锌粉反应的离子方程式__________________。
(5)在蒸发浓缩操作时,要保持一定的酸度,其目的是______。