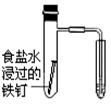
题目内容
仅用下表提供的仪器和药品,就能达到相应实验目的的是、
| 编号 | 仪器 | 药品 | 实验目的 |
| A | 托盘天平(带砝码)、胶头滴管、量筒、烧杯、药匙、玻璃棒 | NaCl固体、蒸馏水 | 配制一定质量份数的NaCl溶液 |
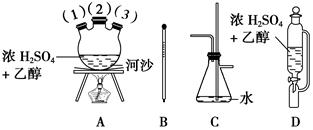
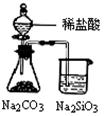
| B | 分液漏斗、烧瓶、锥形瓶、导管及橡皮塞 | 盐酸、大理石、碳酸钠溶液 | 证明非金属性:Cl>C>Si |
| C | 酸式滴定管、胶头滴管、铁架台(带铁夹) | 已知浓度的盐酸、待测NaOH溶液 | 测定NaOH溶液的物质的量浓度 |
| D | 烧杯、分液漏斗、胶头滴管、铁架台 | 待提纯的AlCl3溶液,NaoH溶液 | 提纯混有MgCl2杂质的AlCl3溶液 |
A
试题分析:A、药匙用于取用固体,托盘天平称量固体质量,烧杯用于溶解固体,量筒量取水的体积,玻璃棒用于搅拌,可以配制一定质量分数的溶液,正确;B、该实验可以证明盐酸与碳酸酸性的强弱,不能证明非金属性的强弱,错误;C、缺少指示剂和锥形瓶、碱式滴定管,不能作滴定实验,错误;D、缺少普通漏斗、滤纸,不能过滤,错误,答案选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

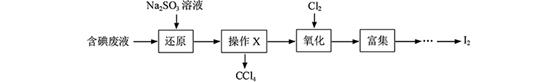
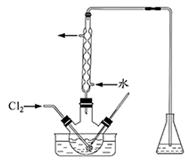
 I2+5SO42—+H2O
I2+5SO42—+H2O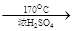 CH2=CH2↑+H2O。
CH2=CH2↑+H2O。