题目内容
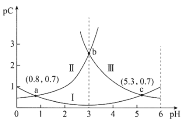
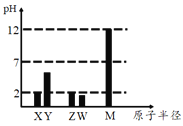
【题目】已知X、Y、Z、W、M 均为短周期元素。25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol/L)溶液的pH和原子半径的关系如图所示。下列说法不正确的是
A.Z元素最高价氧化物的化学式为ZO3
B.简单离子半径大小顺序:X>M
C.简单气态氢化物的稳定性:Z>W>Y
D.X、Z的最简单气态氢化物反应有白烟生成
【答案】A
【解析】
X、Y、Z、W、M均为常见的短周期主族元素,由常温下,其最高价氧化物对应的水化物溶液(浓度均为 0.01mol/L)的pH,X的pH=2,为一元强酸,则为硝酸,X为N元素,Y的半径大于N,且酸性较硝酸弱,应为C元素;Z的原子半径大于C,Z的最高价含氧酸为一元强酸,则Z为Cl,W的原子半径大于Cl,且对应的酸的pH小于2,应为硫酸,W为S元素;M的原子半径最大,且0.01mol/L M的最高价氧化物对应的水化物溶液的pH为12,可知W为Na,以此解答该题。
由以上分析可知X、Y、Z、W、M分别为N、C、Cl、S、Na。
A. Z为Cl,最高化合价为+7价,最高价氧化物的化学式为Z2O7,故A错误;
B. X、M简单离子具有相同的核外电子排布,核电荷数越大,离子半径越小,则半径大小顺序:X>M,故B正确;
C. 非金属越强,简单气态氢化物稳定性越强,所以Cl>S>C,即Z>W>Y,故C正确;
D. X、Z的最简单气态氢化物反应生成氯化铵,有白烟生成,故D正确;
故选A。

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目