题目内容
14.已知草酸镍晶体(NiC2O4•2H2O)难溶于水,工业上从废镍催化剂(成分主要为Ni,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
已知:①相关金属离子生成氢氧化物沉淀的pH如表:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的PH | 3.2 | 8.8 | 5.0 | 9.5 |
③当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)pH的调控范围为5.0≤pH<6.8.
(4)写出“沉镍”时反应的离子方程式Ni2++C2O42-+2H2O=NiC2O4•2H2O,当Ca2+沉淀完全时,溶液中c(F-)>$\sqrt{\frac{1.46×10{\;}^{-10}}{10{\;}^{-5}}}$mol•L-1(写出计算式即可).
分析 废镍催化剂(成分主要为Ni,含有一定量的Al2O3、Fe、SiO2、CaO等),用硫酸溶解,SiO2不与硫酸反应,过滤得到滤液中含有NiSO4、FeSO4、Al2(SO4)3、CaSO4及过量的硫酸,试剂a是一种绿色氧化剂,所以加入 的是H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH,使pH大于5.0小于6.8,Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤除去,滤液中含有NiSO4、CaSO4,向滤液中加入NH4F,除去Ca 2+,过滤,再向滤液中加入(NH4)2C2O4,得到草酸镍沉淀,再过滤、洗涤、干燥得草酸镍晶体,据此答题.
解答 解:废镍催化剂(成分主要为Ni,含有一定量的Al2O3、Fe、SiO2、CaO等),用硫酸溶解,SiO2不与硫酸反应,过滤得到滤液中含有NiSO4、FeSO4、Al2(SO4)3、CaSO4及过量的硫酸,试剂a是一种绿色氧化剂,所以加入 的是加入H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH,使pH大于5.0小于6.8,Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤除去,滤液中含有NiSO4、CaSO4,向滤液中加入NH4F,除去Ca 2+,过滤,再向滤液中加入(NH4)2C2O4,得到草酸镍沉淀,再过滤、洗涤、干燥得草酸镍晶体,
(1)根据影响化学反应速率的因素可知,提高浸出率,可把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等,
故答案为:把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等;
(2)根据上面的分析可知,试剂a是H2O2,所以“氧化”时反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)根据表中的数据可知,pH为5.0时,Fe3+、Al3+沉淀完全,pH为6.8时Ni2+开始沉淀,所以pH的调控范围为5.0~6.8,
故答案为:5.0≤pH<6.8;
(4)“沉镍”时反应的离子方程式为Ni2++C2O42-+2H2O=NiC2O4•2H2O,当Ca2+沉淀完全时,即c(Ca2+)<10-5mol/L,根据Ksp(CaF2)=1.46×10-10,可知溶液中c(F-)>$\sqrt{\frac{1.46×10{\;}^{-10}}{10{\;}^{-5}}}$mol/L,
故答案为:Ni2++C2O42-+2H2O=NiC2O4•2H2O;$\sqrt{\frac{1.46×10{\;}^{-10}}{10{\;}^{-5}}}$mol/L.
点评 本题考查制备方案,涉及化学工艺流程、对操作与试剂的分析评价、化学方程式书写、原电池与电解原理等,是对学生综合能力的考查,需要学生具备扎实的基础与迁移运用能力,难度中等.

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案| 元素 | 相关信息 |
| X | 所有元素中原子半径最小的元素 |
| Y | 地壳中含量最多的元素 |
| Z | 短周期中原子半径最大的金属元素 |
| M | 与Y同主族 |
(2)X、Z可形成化合物ZX,ZX的电子式为Na+[:H]-(用元素符号表示),ZX与盐酸反应.每生成1molX2时转移电子的物质的量为1mol
(3)实验室中检验N的简单离子的试剂是稀硝酸和硝酸银溶液,反应的离子方程式为Ag++Cl-=AgCl↓
(4)M的氢化物5.6L(标准状况下)完全燃烧生成气态氧化物后恢复到室温,放出的热量为127.6kJ,该条件下反应的热化学方程式为2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-510.4kJ/mol.
A.氟利昂 B.SO2C.NO2D.CO2
| 环境问题 | 造成环境问题的主要物质 |
| 温室效应 | |
| 酸雨 | |
| 南极臭氧层空洞 | |
| 光化学烟雾 |
 ;NH3的稳定性比PH3强(填写“强”或“弱”).
;NH3的稳定性比PH3强(填写“强”或“弱”).
 NH3•H2O
NH3•H2O NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除;.
NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除;.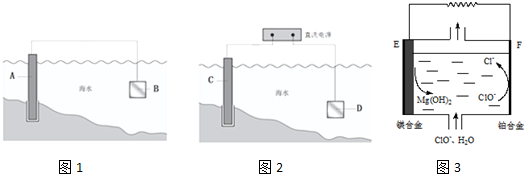

 实验室配制500mL 0.5mol•L-1的NaCl溶液,有如下操作步骤:
实验室配制500mL 0.5mol•L-1的NaCl溶液,有如下操作步骤: