题目内容
2.反应4A(g)+5B(g)?4C(g)+6D(g)△H<0,在一定温度下达到化学平衡状态时,下列说法正确的是( )| A. | 2 v(C)正=3v(D)逆 | |
| B. | 若升高温度最终能生成更多的C和D | |
| C. | 单位时间里有4n mol A消耗,同时有5n mol B生成 | |
| D. | 容器里A、B、C、D的浓度比一定是4:5:4:6 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、不同物质的正逆反应速率之比不等于计量数之比,如果3 v(C)正=2v(D)逆,就是平衡状态,故A错误;
B、升高温度平衡逆向移动,C和D的量减少,故B错误;
C、单位时间里有4n mol A消耗,等效于5n mol B消耗,同时有5n mol B生成,正逆反应速率相等,达平衡状态,故C正确;
D、当体系达平衡状态时,A、B、C、D的浓度比可能是4:5:4:6,也可能不是,与各物质的初始浓度及转化率有关,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.某有机物X的结构简式如图所示,则下列有关说法中正确的是( )
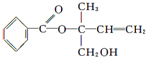

| A. | X的分子式为C12H14O3 | |
| B. | X在一定条件下能发生加成、加聚、取代、消去等反应 | |
| C. | 在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 | |
| D. | 可用酸性高锰酸钾溶液区分苯和X |
13.下列方程式的书写或描述正确的是( )
| A. | 用碳酸钠溶液浸泡锅炉水垢:CaSO4+CO32-═CaCO3↓+SO42- | |
| B. | 热化学方程式C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(g);△H=-1256kJ/mol,表示乙炔的燃烧热为1256kJ/mol | |
| C. | 铂电极电解MgCl2饱和溶液:MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ | |
| D. | H+(aq)+OH(aq)═H2O(1);△H=-57.3 kJ/mol,表示含1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量 |
10.下列各组物质中,属于同系物的是( )
| A. | 甲醇、乙二醇 | B. | 甲酸乙酯和乙酸甲酯 | ||
| C. | 蚁酸和乙酸 | D. | 苯酚( -OH)和甲苯( -OH)和甲苯( -CH3) -CH3) |
17.下列关于物质性质的比较,不正确的是( )
| A. | 金属性由强到弱:Na>Mg>Al | |
| B. | 离子半径由大到小:Na+>S2->O2- | |
| C. | 离子的还原性由强到弱:S2->Cl->F- | |
| D. | 酸性由强到弱:HClO4>HBrO4>HIO4 |
7.下列说法不正确的是( )
| A. | 一定温度下,反应2H2O(l)═2H2(g)+O2(g)的△H>0△S>0 | |
| B. | 水解反应NH4++H2O?NH3•H2O+H+达到平衡后,升高温度平衡逆向移动 | |
| C. | 对于反应2H2O2═2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 | |
| D. | AgCl悬浊液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量NaCl晶体,平衡逆向移动,Ksp减小 |
14.合金是一类用途广泛的金属材料.下列物质不属于合金的是( )
| A. | 黄金 | B. | 青铜 | C. | 钢铁 | D. | 不锈钢 |
11.有一种铁的化合物俗称铁红,常用作红色油漆和外墙涂料,这种铁的化合物是( )
| A. | Fe2O3 | B. | Fe(OH)3 | C. | FeO | D. | Fe3O4 |
12.已知锌与稀盐酸反应放热.某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气.
所用稀盐酸浓度为1.00mol•L-1、2.00mol•L-1,锌有细颗粒与粗颗粒两种规格,用量为6.50g.实验温度为298K、308K,每次实验稀盐酸的用量为25.0mL.
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
(2)实验①记录如下:
①计算在30-40s范围内盐酸的平均反应速率v(HCl)=0.056mol/(L•s).(忽略溶液体积变化,不需要写出计算过程).
②反应速率最大的时间段(即0~10S、10~20S、20~30S、30~40S、40~50S、…)为40~50s,可能原因是反应放热;
③反应速率最小的时间段为90~100s,可能原因是盐酸浓度降低.
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入等体积的下落溶液以减慢反应速率:
A.蒸馏水B.CuCl2溶液C.NaCl溶液
你认为他上述做法中可行的是AC(填相应字母).
所用稀盐酸浓度为1.00mol•L-1、2.00mol•L-1,锌有细颗粒与粗颗粒两种规格,用量为6.50g.实验温度为298K、308K,每次实验稀盐酸的用量为25.0mL.
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
| 编号 | T/K | 锌规格 | 盐酸浓度/mol•L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响;(Ⅱ)实验①和 ③探究温度对该反应速率的影响;(Ⅲ)实验①和 ④探究锌规格(粗、细)对该反应速率的影响. |
| ② | 298 | |||
| ③ | 308 | |||
| ④ | 298 |
| 时间(S) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积(mL) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(即0~10S、10~20S、20~30S、30~40S、40~50S、…)为40~50s,可能原因是反应放热;
③反应速率最小的时间段为90~100s,可能原因是盐酸浓度降低.
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入等体积的下落溶液以减慢反应速率:
A.蒸馏水B.CuCl2溶液C.NaCl溶液
你认为他上述做法中可行的是AC(填相应字母).