��Ŀ����
����Ŀ����ҵ�������β���к���N2O��NO��NO2�ȵ��������ǿ�����Ⱦ����е��������β���账��������ŷš�
I.��ҵ�����
��1�������������ǹ�ҵ������Ļ�����Ӧ��д�����������Ļ�ѧ����ʽΪ___��
II.������������������
��2��N2O�Ĵ�����N2O�����������а��������ĸ���������ִ�����ʹN2O�ֽ⣬N2O�ֽ�Ļ�ѧ����ʽΪ___��
��3��NO��NO2�Ĵ�������֪NO��NO2�ڼ���Һ�п��Է������·�Ӧ��NO+NO2+2OH-=2NO2-+H2O��2NO2+2OH-=NO2-+NO3-+H2O
�����д�ʩ�����β����NO��NO2ȥ���ʵ���___������ĸ����
A���ӿ�ͨ��β��������
B����������Һ�����ķ�ʽ����β��
C������β�������ж��ڲ�������NaOH��Һ
D����β��ͨ��NaOH��Һ��ͬʱͨ������������β����������
�� ��NO��NO2��β������NaOH��Һ���գ����պ����Һ��___�����ˣ��õ�NaNO2���塣
�� ���պ��ŷŵ�β���к����ϸߵĵ���������___���ѧʽ����
��4����NaClO��Һ����β������NaClO��Һ����NaOH��Һ��������β���������β����NO��ȥ���ʡ�����������ͬ��NOת��ΪNO3-��ת������NaClO��Һ��ʼpH����ϡ������ڣ��ı仯��ͼ��ʾ��
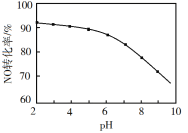
��������NaClO��Һ�У�HClO����NO����NO3-ʱ������Ӧ�����ӷ���ʽΪ___��
��NaClO��Һ�ij�ʼpHԽС��NOת����Խ�ߡ���ԭ����___��
���𰸡�4NH3+5O2![]() 4NO+6H2O 2N2O
4NO+6H2O 2N2O![]() 2N2+O2 BCD Ũ�����ᾧ NO 3HClO+2NO+H2O=3Cl-+2NO3-+5H+ ��ҺpHԽС����Һ��HClO��Ũ��Խ������NO������Խǿ
2N2+O2 BCD Ũ�����ᾧ NO 3HClO+2NO+H2O=3Cl-+2NO3-+5H+ ��ҺpHԽС����Һ��HClO��Ũ��Խ������NO������Խǿ
��������
I.��1�����������Ļ�ѧ����ʽΪ4NH3+5O2![]() 4NO+6H2O��
4NO+6H2O��
II.��2��N2Oֻ����N��O����Ԫ�أ�����ֽ����Ϊ��������������N2O�ķֽⷽ��ʽΪ2N2O![]() 2N2+O2��
2N2+O2��
��3����A. �ӿ�ͨ��β�������ʿ��ܻ�ʹ�������ղ���ȫ�������ȥ���ʣ�A���������⣻
B. ��������Һ�����ķ�ʽ����β������������������Һ��ĽӴ���������β��ȥ���ʣ�B�������⣻
C. ����β�������ж��ڲ�������NaOH��Һ���������β��ȥ���ʣ�C�������⣻
D. ��β��ͨ��NaOH��Һ��ͬʱͨ����������Դٽ�NO�����գ��Ӷ����β��ȥ���ʣ�D�������⣻
�ʴ�ѡBCD��
�ں�NO��NO2��β������NaOH��Һ���գ����պ����Һ������Ũ������ȴ�ᾧ�����˺�ɵõ���Ӧ�ľ��壻
������NO2��ˮ��Ӧ������NO��NO����ˮ��Ӧ���������պ��ŷŵ�β���к����ϸߵĵ���������NO��
��4����������NaClO��Һ�У�ClԪ����HClO����ʽ���ڣ�HClO����NO����NO3-ʱ������Ӧ�����ӷ���ʽΪ3HClO+2NO+H2O=3Cl-+2NO3-+5H+��
����ҺpHԽС����Һ��HClO��Ũ��Խ������NO������Խǿ��