题目内容
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的常用试剂是___,证明Fe3+存在的现象是____,配制含Fe2+的溶液时,常常向溶液中加入少量___,使被氧气氧化形成的Fe3+还原为Fe2+。
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:___。
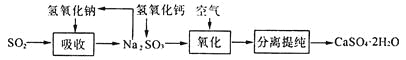
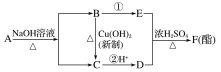
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

A.请写出上述实验中加入或生成的有关物质的化学式。
①___,②___,③___,④____,⑤____,⑥_____。
B.请写出相关反应的化学方程式。_______。
【答案】KSCN溶液 溶液变成红色 铁粉 2FeCl3+Cu=2FeCl2+CuCl2 Fe FeCl2 Fe和Cu HCl FeCl2 Cl2 CuCl2+Fe=FeCl2+Cu、2FeCl3+Fe=3FeCl2、Fe+2HCl=FeCl2+H2↑、2FeCl2+Cl2=2FeCl3
【解析】
(1)检验溶液中Fe3+存在通常用KSCN溶液,溶液变红说明Fe3+存在;Fe2+容易被空气中的氧气氧化,为了防止亚铁离子被氧化,结合不能引入新杂质分析判断;
(2)铜与氯化铁反应生成氯化铜、氯化亚铁;
(3)反应中含有氯化亚铁、氯化铜和未反应的氯化铁,由工艺流程可知,滤渣③中含有金属铜,应是废液与过量的Fe反应,滤液②中含有氯化亚铁,滤渣③中含有金属铜、未反应的铁,加入盐酸,过滤,回收铜,滤液⑤中含有氯化亚铁,与滤液②合并,通入氯气可以得到氯化铁,据此分析解答。
(1)检验溶液中Fe3+存在通常用KSCN溶液,取少量溶液于试管中,滴加KSCN溶液,溶液变红说明存在Fe3+;配制含Fe2+的溶液时,为了防止亚铁离子被氧化,且不能引入新杂质,常加入铁粉(铁钉也可),使被氧气氧化形成的Fe3+还原为Fe2+,故答案为:KSCN溶液;溶液变红;铁粉;
(2)氯化铁与铜反应生成氯化亚铁与氯化铜,反应的化学方程式为:2FeCl3+Cu═2FeCl2+CuCl2,故答案为:2FeCl3+Cu═2FeCl2+CuCl2;
(3)A.废液中含有氯化亚铁、氯化铜和未反应的氯化铁,由工艺流程可知,滤渣③中含有金属铜,应是废液与过量的Fe反应,滤液②中含有氯化亚铁,滤渣③中含有金属铜和未反应的铁,加入盐酸,滤液⑤中也含有氯化亚铁,与滤液②合并后通入氯气可以得到氯化铁,故答案为:Fe;FeCl2;Fe、Cu;HCl;FeCl2;Cl2;
B.废液中加入铁粉,发生CuCl2+Fe=Cu+FeCl2、2FeCl3+Fe=3FeCl2;滤渣中含有铁、铜,加入盐酸,铁与盐酸反应,化学方程式为Fe+2HCl=FeCl2+H2↑,氯化亚铁与氯气的反应,化学方程式为2FeCl2+Cl2=2FeCl3,故答案为:CuCl2+Fe=Cu+FeCl2、2FeCl3+Fe=3FeCl2、Fe+2HCl=FeCl2+H2↑、2FeCl2+Cl2=2FeCl3。

【题目】雾霾天气肆虐给人类健康带来了严重影响.燃煤和汽车尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO![]() 2CO2(g)+N2(g)△H<0
2CO2(g)+N2(g)△H<0
①反应的速率-时间图像如图甲所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如图乙所示。以下说法正确的是___________(填对应字母)。
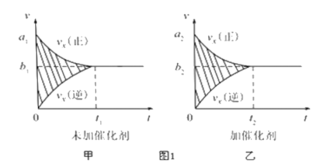
A. a1>a2 B.b1<b2 C.t1>t2 D.图乙中阴影部分面积更大E.图甲中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是_________(填代号)

(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
已知:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
2NO2(g)![]() N2O4(g)△H=﹣56.9kJ/mol
N2O4(g)△H=﹣56.9kJ/mol
H2O(g)=H2O(l)△H=﹣44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:______________。
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2OCO+3H2,该反应在不同温度下的化学平衡常数如表:
温度/℃ | 800 | 1000 | 1200 | 1400 |
平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
①该反应是_________反应(填“吸热”或“放热”)。
②T℃时,向1L密闭容器中投入lmolCH4和lmolH2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O![]() CO+3H2的平衡常数K=______________。
CO+3H2的平衡常数K=______________。