题目内容
2010年10月1日,我国在西昌卫星发射中心成功发射“嫦娥二号”。嫦娥二号火箭推进器以联氨(N2H4)为燃料、过氧化氢为助燃剂。已知下列各物质反应的热化学方程式为
N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH1=-533.23 kJ·mol-1
H2O(g)=H2O(l);ΔH2=-44 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g);ΔH3=-196.4 kJ·mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH1=-533.23 kJ·mol-1
H2O(g)=H2O(l);ΔH2=-44 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g);ΔH3=-196.4 kJ·mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
| A.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);ΔH=+817.63 kJ·mol-1 |
| B.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);ΔH=-641.63 kJ·mol-1 |
| C.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);ΔH=-641.63 kJ·mol-1 |
| D.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);ΔH=-817.63 kJ·mol-1 |
B
本题考查热化学反应方程式的书写和简单相关计算。
N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);
ΔH=-533.23 kJ·mol-1+(-196.4 kJ·mol-1)+2×(-44 kJ·mol-1)=-817.63 kJ·mol-1。
N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);
ΔH1=-533.23 kJ·mol-1+(-196.4 kJ·mol-1)-2×(-44 kJ·mol-1)=-641.63 kJ·mol-1
B选项正确。
N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);
ΔH=-533.23 kJ·mol-1+(-196.4 kJ·mol-1)+2×(-44 kJ·mol-1)=-817.63 kJ·mol-1。
N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);
ΔH1=-533.23 kJ·mol-1+(-196.4 kJ·mol-1)-2×(-44 kJ·mol-1)=-641.63 kJ·mol-1
B选项正确。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1 
 2NO2(g) △H= -113.0 kJ·mol-1
2NO2(g) △H= -113.0 kJ·mol-1 

 的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。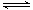 2NO(g) △H
2NO(g) △H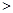 0
0 2HgO(s)ΔH=-181.6 kJ·mol-1
2HgO(s)ΔH=-181.6 kJ·mol-1 2NH3的能量变化如图所示,该反应的热化学方程式是( )
2NH3的能量变化如图所示,该反应的热化学方程式是( )
 2NH3(l) ΔH=2(a-b-c)kJ·mol-1
2NH3(l) ΔH=2(a-b-c)kJ·mol-1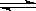 CO2(g) + H2(g)
CO2(g) + H2(g)