题目内容
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.常温常压下,1.06g Na2CO3含有的Na+离子数为0.01NA
B.标准状况下,22.4L酒精含有的分子数为NA
C.在常温常压下,28gN2与CO混合物气体中所含的分子数目一定为NA
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
【答案】C
【解析】
A、1.06g碳酸钠的物质的量为![]() =0.01mol,而碳酸钠中含2个钠离子,故0.01mol碳酸钠中含钠离子为0.02NA个,故A错误;
=0.01mol,而碳酸钠中含2个钠离子,故0.01mol碳酸钠中含钠离子为0.02NA个,故A错误;
B、标准状况下,酒精为液体,不能根据气体摩尔体积来计算其物质的量,故B错误;
C、氮气和CO的摩尔质量均为28g/mol,故28g混合气体的物质的量为![]() =1mol,故分子数N=nNA=NA个,故C正确;
=1mol,故分子数N=nNA=NA个,故C正确;
D、溶液的体积不明确,溶液中氯离子的个数无法计算,故D错误;
故选C。

【题目】Ⅰ.NOx、CO、SO2等大气污染气体的处理和利用是世界各国研究的热点问题。
(1)已知:
a.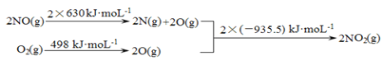
b.2NO(g)+O2(g)![]() 2NO2(g) ΔH1
2NO2(g) ΔH1
2SO2(g)+O2(g)![]() 2SO3(g) ΔH2=-196.6 kJ·mol-1
2SO3(g) ΔH2=-196.6 kJ·mol-1
①ΔH1 =___kJ·mol-1。
②写出NO2气体与SO2气体反应生成SO3气体和NO气体的热化学方程式____。
(2)煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低了脱硫效率。发生的两个相关反应的热化学方程式如下:
反应Ⅰ:CaSO4(s)+CO(g)![]() CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1
反应Ⅱ:CaSO4(s)+4CO(g)![]() CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1
CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1
(资料:①反应Ⅰ和反应Ⅱ同时发生,②反应Ⅰ的速率大于反应Ⅱ的速率)
请回答下列问题:
①下列反应过程能量变化示意图正确的是____。
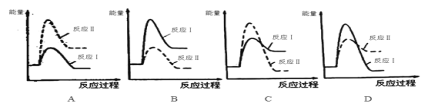
Ⅱ.可逆反应mA(g)+nB(g)![]() pC(g)+gD(g)的v—t图像如图甲所示,若其他条件不变,只在反应前加入合适的催化剂,其v-t图像如乙所示。下列说法正确的是___。
pC(g)+gD(g)的v—t图像如图甲所示,若其他条件不变,只在反应前加入合适的催化剂,其v-t图像如乙所示。下列说法正确的是___。
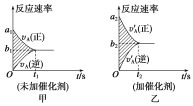
①a1=a2 ②a1<a2 ③b1=b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧图Ⅱ中阴影部分面积更大
Ⅲ.在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表:
T/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
请回答下列问题:
①试比较K1、K2的大小,K1____K2(填”>”“=“或”<”)。
②400℃时,反应2NH3(g)![]() N2(g)+3H2(g)的平衡常数K为____。当测得NH3、N2、H2的浓度分别为3molL1、2molL1、1molL1时,则该反应的v正(N2)___v逆(N2)(填”>”“=“或”<”)。
N2(g)+3H2(g)的平衡常数K为____。当测得NH3、N2、H2的浓度分别为3molL1、2molL1、1molL1时,则该反应的v正(N2)___v逆(N2)(填”>”“=“或”<”)。